Ацетальде-гид
Cтраница 1
Ацетальде-гид не относится к виниловым мономерам, которым был посвящен наш доклад. [1]
Так, ацетальде-гид ( 151; R Н, R СН3) и аммиак дают 4-пиколин и 3-этил - 4-метилпиридин, который образуется, вероятно, при конденсации соединения ( 153) с другой молекулой ацетальдегида и последующем дегидрировании. Таким же путем, по-видимому, через соединение ( 154) образуются 2-пиколин и 2-метил - 5-этилпиридин. Смесь ацетальдегида, бензальдегида ( см. 151; R Н, R С6Н5) и аммиака дает 4-фенилпиридин; бензальацетофенон и ацетофенон ( ср. [2]
После отгонки ацетальде-гида кротоновый альдегид перегоняют в виде азеотропной смеси с 10 % воды. [3]
Вычислите количество вещества ацетальде-гида, который образуется по реакции Кучерова из 5 кг ацетилена, содержащего 0 2 % примеси. [4]
Так, действие ацетальде-гида на 2-метилпентен - 1-ол - 4 ( VIII) в присутствии конц. [5]
Уксусный альдегид, или ацетальде-гид, получается в промышленном масштабе различными методами. В более старом способе исходят из ацетилена ( метод основан на реакции Кучерова, см. стр. [6]
Для анализа разбавленных водных растворов ацетальде-гида, кретонового альдегида и этилового спирта, получающихся в процессе каталитического окисления этилена в ацеталь-дегид, применен хроматограф Хром-1 с пламенно-ионизационным детектором, нечувствительным к воде. Подобрана смешанная жидкая фаза ( полиэтиленгликоль-1000 р р - тиоди-пропионитрил), на которой вода не мешает разделению и количественному определению указанных выше веществ. Длина колонки 85 см, температура 70 С, расход азота 42 мл / мин. Минимальная определяемая концентрация альдегидов и спирта составляет 0 005 % при объеме пробы 0 02 мл. [7]
 |
Телоиеризация винилэтилового эфира диэтилацеталем уксусного альдегида. [8] |
Так, при присоединении дибутилацеталя ацетальде-гида к винплэтиловому эфиру был получен не только 1-этокси - 1 3-дибутоксибутан, но и 1 1 3-трибутоксибутан, образование которого следует отнести за счет переацетализации. Интересно, что при взаимодействии диэтилацеталя ацетальдегида с - бромвинилбутиловым эфиром продуктов переацетализации не наблюдается, образуется только 1 3-диэтоксп - 1-бутокси - 2-бромбутан [808], что можно объяснить снижением подвижности алкоксильных групп в а-бромацеталях за счет - / - эффекта брома. [9]
Для анализа разбавленных водных растворов ацетальде-гида, кротонового альдегида и этилового спирта, получающихся в процессе каталитического окисления этилена в ацеталь-дегид, применен хроматограф Хром-1 с пламенно-ионизационным детектором, нечувствительным к воде. Подобрана смешанная жидкая фаза ( полиэтиленгликоль-1000 р р - тиоди-пропионитрил), на которой вода не мешает разделению и количественному определению указанных выше веществ. Длина колонки 85 см, температура 70 С, расход азота 42 мл / мин. Минимальная определяемая концентрация альдегидов и спирта составляет 0 005 % при объеме пробы 0 02 мл. [10]
III) расщепляется с образованием свободного ацетальде-гида. [11]
Треонин получается взаимодействием глицина с ацетальде-гидом. Глицин предварительно превращают во внутрикомплекс-ную медную соль, так как при этом резко повышается реакционная способность метиленовой группы. [12]
 |
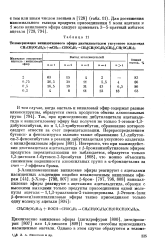
Диаграммы скоростей образования окиси этилена и углекислого газа при окисл жни этилена и его смесей с альдегидами на серебре при 220. [13] |
Все кислородсодержащие соединения ( формальдегид, ацетальде-гид и окись этилена) захватываются поверхностью контакта. Это подтверждается изотопным анализом СО г, образующегося при выжигании этих соединений, адсорбированных на поверхности контакта, а также несоответствием скорости их расходования и окисления в углекислый газ. [14]
Гидратацией ацетилена или его гомологов получают ацетальде-гид или соответствующие кетоны. В основе эти процессов лежит открытая М. Г. Кучеровым ( 1881 г.) [10] реакция гидратации ацетилена в ацетальдегид в присутствии H SO4 с добавкой солей ртути. Хотя эта реакция известна давно и проводится в заводском масштабе, но механизм ее недостаточно изучен и в настоящее время. [15]
Страницы: 1 2 3 4