Аминокомпонент
Cтраница 2
О возможности применения натриевых солей аминокислот или пептидов в качестве аминокомпонентов указаний нет - но можно было бы ожидать выходов ниже 45 - 77 %, которые получались с эфирами аминокислот и пептидов в инертных растворителях. Влияние воды на стадию образования амида не установлено. [16]
Как видно из приведенной схемы, активированный эфир реагирует с аминокомпонентом, давая защищенный дипептид. [17]
Этот активированный эфир может вступать в реакцию с еще не прореагировавшим аминокомпонентом, что приводит к появлению пептидов с большой молекулярной массой. [18]
Обычно аквимолярные количества защищенной аминокислоты, хлор-гидрата, броыгидрата или бензолсульфоната аминокомпонента, третичного основания ( триетнламина, этилдиизопропиламина шш Ж - метилмор-фолина) и ДЩТС растворяют в подходящем растворителе при О С, перемешивают 4 - 2 ч и оставляют на 42 ч при комнатной температуре. [19]
 |
Защитные группы для имидазольной функции гистидина. [20] |
К тому же существует опасность, что частичное детозилирование при нуклеофильном воздействии аминокомпонента приведет к образоианию № - тозилпроизводного пептида. Пиридилдифенилметильная группа [178] аналогично давно известной NIm-тритильной группе [181] может отщепляться гидрогенолизом или ацидоли-зом. [21]
Карбоксизащитные группы этого типа могут применяться для пептидных синтезов только в определенных условиях, так как аминокомпоненты с активированными карбоксильными группами могут вступать в реакцию не только с карбоксильными компонентами, но и давать нежелательные побочные продукты в результате внутри - и межмолекулярной самоконденсации. Для того чтобы обеспечить однозначное течение реакции, в пептидном синтезе применяют карбоксильные компоненты, имеющие более высокий потенциал ацилирования, чем активированная карбок-сизащитная группа аминокомпонента. [22]
Бензиловые эфиры простых N-защищенных аминокислот получают сравнительно редко, так как их использование в синтезе пептидов в качестве аминокомпонента должно предусматривать снятие N-защитной группы. Бензиловые эфиры указанного типа обычно получают путем этерификации N-защищенных аминокислот бензиловым спиртом в присутствии каталитических количеств толуолсульфокислоты [149, 596], хлористого сульфурила [2278] или эквивалентного количества хлористого тионила [1315] в бензоле или смлш-тетрахлорэтане. [23]
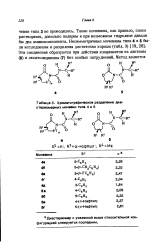 |
Хроматографическое разделение диа стереомерных мочевин типа 4 и 5. [24] |
Такие мочевины, как правило, плохо растворимы, довольно полярны и при возможном гидролизе давали бы два аминокомпонента. Эти соединения образуются при действии изоцианатов на лактамы ( 6) и оксазолидиноны ( 7) без особых затруднений. [25]
Бензиловые эфиры простых N-защищенных аминокислот получают сравнительно редко, так как их использование в синтезе пептидов в качестве аминокомпонента должно предусматривать снятие N-защитной группы. Бензиловые эфиры указанного типа обычно получают путем этерификации N-защищенных аминокислот бензиловым спиртом в присутствии каталитических количеств толуолсульфокислоты [149, 596], хлористого сульфурила [2278] или эквивалентного количества хлористого тионила [1315] в бензоле или силш-тетрахлорэтане. [26]
Некоторые азиды могут быть выделены путем осаждения при добавлении ледяной воды и затем, после растворения в подходящем растворителе, введены в реакцию с аминокомпонентом. Эти операции следует проводить при низких температурах ввиду нестабильности азидов и связанной с этим опасности взрыва. [27]
С этой целью силикагель пропитывается полярным растворителем ( ДМФ, ацетонитрил, гексаметилтри-амид фосфорной кислоты ( ГМТАФ) и др.) и адсорбционио нагружается аминокомпонентом. Фиксированный на силикагеле аминокомпонент взаимодействует далее с пентафторфениловыми эфирами Вос-аминокислот, суспендированными в гексане или петролейном эфире. Пептидный синтез происходит в тонком слое полярного растворителя на поверхности силикагеля, в котором реакционные партнеры находятся в высокой концентрации. Избыток активированного эфира удаляют промыванием диэтиловым эфиром. После отщепления Вос-группы с помощью НС1 в дибутиловом эфире проводят следующую стадию конденсации. [28]
Вообще говоря, спиртовой гидроксил можно не защищать, если серии ( R Н), треонин ( R СН3) или гидроксипролин является составной частью аминокомпонента. [29]
Благодаря такой последовательности реакций, когда растущая полипептидная цепь находится попеременно то в твердой, то в жидкой фазе, можно на определенных этапах полностью удалить как непрореагировавший аминокомпонент, так и недеблокированный пептид. [30]
Страницы: 1 2 3 4