Логарифм - константа - равновесие
Cтраница 1
 |
Растворимость BiOCl в азотной [ IMAGE ] Растворимость ВЮВг в азотной кислоте. кислоте. [1] |
Логарифм константы равновесия численно равен величине отрезка отсекаемого прямой на оси ординат. [2]
Логарифмы констант равновесия и скоростей реакций при заданной температуре согласно уравнениям (2.2) и (2.6) линейно связаны с изменениями свободной энергии реакции ( Д5) и свободной энергии активации ( Д3) соответственно. [3]
Логарифм константы равновесия Kf и давление насыщенных паров psj являются известными температурными функциями. [4]
Логарифмы констант равновесия таутомерных веществ связаны между собой линейной зависимостью. Из первой зависимости следует, что таутомерное равновесие всегда смещено в сторону менее кислотной ( или менее основной) в данной среде формы. [5]
Поэтому логарифм константы равновесия lg К или логарифм константы скорости gk является удобной химической мерой изменения свободной энергии в пределах серии однотипных реакций. [6]
Расчеты логарифмов констант равновесия и изобарных потенциалов были проведены приближенным методом автора без учета влияния изменения теплоемкостей реагирующих веществ с изменением температуры. [7]
Величина логарифма константы равновесия и равновесные концентрации с повышением температуры падают. Реакции гидрогенолиза алифатических сульфидов и меркаптанов протекают без изменения объема, поэтому равновесная глубина гидрогенолиза этих соединений не зависит ни от их концентрации в подвергаемом гидроочистке нефтепродукте, ни от общего давления. [8]
Напротив, логарифм константы равновесия второй стадии реакции замещения иодид-ионом, по-видимому, обратно пропорционален диэлектрической проницаемости растворителя. [10]
 |
Зависимость между lg A X / A H.| Завнспмостг / между lg К / КЪ1 реакции обратимого окисления соединении С51ТбРоСзН4Х и XQ-JLtFeCsFUY. [11] |
Интересно сравнить логарифмы констант равновесия окисления и восстановления с константами а Гаммстта. [12]
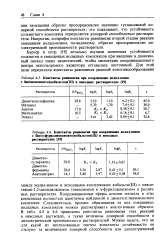
При сравнении логарифмов констант равновесия, рассчитанных по работе [89] и приведенных в литературе, видно, что значения 1пЛГр попадают в рассчитанный доверительный интервал для реакции ( а) до температуры 1273 К, а для реакции ( б) при температурах от 973 до 1173 К. [13]
Прямолинейная зависимость логарифмов констант равновесия от обратной температуры ( рис. 7) характеризует взаимодействие сульфидов с серной кислотой как активационный экзотермический процесс. [14]
С для логарифма константы равновесия получены значения lg k - 1 21 - т - 1 02, что соответствует теплоте реакции перехода ДЯ - 1 ккал / моль. [15]
Страницы: 1 2 3 4