Логарифм - константа - равновесие
Cтраница 4
В рассмотренном примере удельное значение поправки к величине логарифма константы равновесия невелико. Это связано с тем, что величина константы равновесия для исследованной реакции очень велика, равно как и велико по абсолютной величине значение изобарного потенциала реакции. [46]
Совместное решение уравнений (2.13) и (2.14) при известных дает логарифм константы равновесия. Данные по стандартным энергиям Гиббса образования различных веществ имеются в термодинамических справочниках. [47]
 |
Изменение констант равновесия в зависимости от температуры 7. [48] |
АЯ и AS0 в зависимости от температуры, то логарифм константы равновесия является линейной функцией величины, обратной абсолютной температуре. [49]
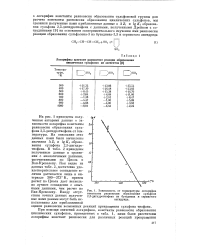 |
Зависимость от температуры логарифма. [50] |
На рис. 1 приведены полученные авторами данные о зависимости логарифма константы равновесия образования сульфона 2 5-дигидротиофена от температуры. На основании этих данных нами были вычислены значения A Z / и lg Kf образования сульфона 2 5-дигидротиофена. В табл. 2 приведены полученные данные в сравнении с аналогичными данными, рассчитанными по Циола и Ван-Кревелену. Как видно из данных табл. 2, достаточно удовлетворительное совпадение величин достигается лишь в интервале 300 - 373 К, причем расчет по Циола дает несколько лучшее совпадение с опытными данными, чем расчет по Ван-Кревелену. Ввиду отсутствия точных данных полученные нами данные могут быть использованы для приближенной оценки равновесия возможных реакций превращения сульфона тиофана. [51]
Следует иметь в виду, что потенциал полуволны пропорционален логарифму константы равновесия ( для обратимых процессов) или константы скорости лимитирующей стадии ( для необратимых процессов) окислительно-восстановительной реакции. [52]
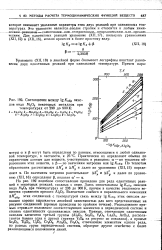 |
Соотношение между Ig / C06p окислов вида М2О3 некоторых металлов при. [53] |
Уравнение ( XII, 18) в линейной форме связывает логарифмы констант равновесия двух однотипных реакций при одинаковой температуре. [54]
Совместное решение уравнений (2.13) и (2.14) при известных AfG дает логарифм константы равновесия. Данные по стандартным энергиям Гиббса образования различных веществ имеются в термодинамических справочниках. [55]
В табл. 384 даны значения коэффициентов в интерполяционных формулах для логарифмов констант равновесия, приведенных в таблицах термодинамических свойств газов. [56]
С целью еще большего упрощения работы по вычислению приближенных значений логарифма констант равновесия автором разработана методика и на ее основе составлена вспомогательная таблица, позволяющая с исключительной простотой и легкостью получить значения логарифма константы равновесия любой химической реакции. [57]
Для процесса превращения Мгь в Мпж логарифм константы складывается из логарифмов констант равновесия всех промежуточных переходов. [58]
Для стандартной температуры величина этой поправки равна нулю, и значения логарифмов констант равновесия по приближенному и точному методам расчета совпадают. [59]
К аналогичным выводам приводит и изучение изменения энтропии, а также логарифма константы равновесия образования. [60]
Страницы: 1 2 3 4