Логарифм - константа - равновесие
Cтраница 3
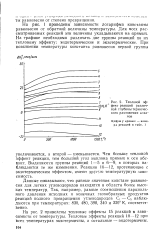 |
Тепловой эффект реакций различной глубины термического разложения алка. [31] |
На рис. 1 приведены зависимости логарифма константы равновесия от обратной величины температуры. Для всех рассматриваемых реакций эти величины укладываются на прямых. На графике необходимо различать две группы реакций по их тепловому эффекту: эндотермические и экзотермические. [32]
В табл. 9 приводятся значения логарифма констант равновесия для этих реакций при различных температурах. На рис. 1 и 2 представлены диаграммы зависимости lg Кр от 1 IT для некоторых случаев первых двух перечисленных выше реакций с участием сернистых соединений различных типов. [33]
Кривая проведена по данным для логарифмов констант равновесия, вычисленных по Касселю. [34]
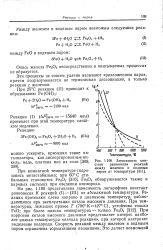 |
Зависимость констант равновесия реакций между железом и водяным паром от температуры. [35] |
На рис. 1.100 представлена зависимость логарифмов констант равновесия К реакций ( I) - ( III) от абсолютной температуры. Реакции протекают слева направо в диапазоне температур, наблюдающихся при эксплуатации котлов высокого давления. При коррозии котлов высокого давления представляет интерес наиболее низкая температура начала реакции, при которой наступает выделение водорода. Скорость реакций между железом и водяным паром ограничена тормозящими явлениями. [36]
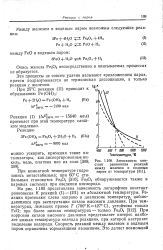 |
Зависимость констант равновесия реакций между железом и водяным паром от температуры. [37] |
На рис. 1.100 представлена зависимость логарифмов констант равновесия К реакций ( I) - ( III) от абсолютной температуры. Реакции протекают слева направо в диапазоне температур, наблюдающихся при эксплуатации котлов высокого давления. При коррозии котлов высокого давления представляет интерес наиболее низкая температура начала реакции, при которой наступает выделение водорода. Скорость реакций между железом и водяным паром ограничена тормозящими явлениями. [38]
Тде рАя - отрицательная величина логарифма константы равновесия для превращения спирта ROH в карбокатион R; / TR - функция кислотности растворителя ( обычно смеси H2SO4 и Н2О; см. гл. ROH помещают в раствор серной кислоты с известным значением Як. [39]
На рис. 24 представлены значения логарифма константы равновесия гидролиза SiFp как функции температуры. Полученные разными методами данные удовлетворительно сходятся между собой. [40]
На рис. 6.3 нанесена также зависимость логарифма константы равновесия образования циангидринов из замещенных бензальде-гидов и синильной кислоты [76] от констант заместителей. Реакционная способность карбонильной группы здесь возрастает с ростом дефицита электронов на карбонильном углероде [ см. (6.24) ], так что наблюдается зависимость от эффектов заместителей, обратная изменению основности карбонильного атома кислорода. [41]
Строят для каждого давления схождения график зависимости логарифма константы равновесия от температуры кипения углеводородов, начиная с м-пентана и кончая гексадеканом. Через точки, соответствующие константам равновесия нормальных парафиновых углеводородов, на этом графике можно провести прямую линию. С этой прямой снимают значения констант равновесия для фракций конденсата в соответствии с их средними температурами кипения. [42]
В настоящей главе приведены полные сводки уравнений логарифмов констант равновесия процессов плавления, испарения и сублимации металлов и некоторых неметаллов, рассчитанных автором на основе точного метода. Все рассчитанные уравнения отвечают потребностям как приближенных, так и точных расчетов. [43]
Для расчета состава равновесной смеси необходимо знать не логарифм константы равновесия, а ее численное значение. [44]
Из табл. 62 видно, что данные для логарифмов констант равновесия, найденные как по эмпирическим уравнениям, так и по спектроскопическим данным, для температур выше 700 К ( 427 С) хорошо согласуются друг с другом. Повидимому, при низких температурах предпочтение следует отдать расчетам по спектроскопическим данным, которые должны правильнее передавать ход констант равновесия с температурой в области экстраполяции. [45]
Страницы: 1 2 3 4