Логарифм - коэффициент - распределение
Cтраница 3
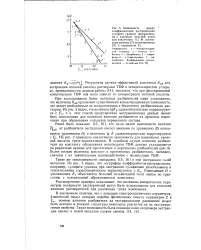
Важнейший результат, полученный в результате анализа выведенных уравнений, - линейность зависимости логарифма коэффициента распределения от обратной температуры по абсолютной шкале - был экспериментально подтвержден в работах Тармонда, Стразерса [15] и Холла [ 161 для ряда примесей в германии и кремнии. Однако в дальнейшем Трамбором с сотрудниками [17, 18] были обнаружены нарушения этой закономерности, например для примеси олова в германии и кремнии. [31]
Показано, что распределение стронция между осадком активной двуокиси марганца и водными растворами метилового, этилового и н-пропилового спиртов удовлетворительно подчиняется уравнению, согласно которому логарифм коэффициента распределения линейно зависит от обратной величины диэлектрической постоянной растворителя. [32]
Исследование комплексообразования иона Fe3 с диоксимом методом распределения было проведено с двл / мя опганическими растворителями: н-амиловым спиртом и хлороформом. Оказалось, что отношение логарифмов коэффициентов распределения не остается постоянным при изменении равновесной концентрации свободного лиганда. Из этого следует, что состав комплексов в водных фазах обеих систем неодинаков. Следовательно, различие в составе этих комплексов может быть обусловлено только наличием в одном из них молекул органического растворителя. [33]
Из рис. 5 видно, что логарифмы коэффициентов распределения, например, сульфата уранила при экстракции сульфатами диоктиламина и триоктиламина удовлетворительно коррелируются с Ет. [35]
На экстрагирование влияют также и другие соединения, в частности посторонние соли, находящиеся в экстрагируемом растворе. На рис. 325 приведены кривые изменения логарифма коэффициента распределения уранилнитрата между водой и ди-этиловым эфиром в присутствии различных нитратов. [36]
На экстрагирование влияют также и Другие соединения, в частности посторонние соли, находящиеся в экстрагируемом растворе. На рис. 325 приведены кривые изменения логарифма коэффициента распределения уранилнитрата между водой и ди-этиловым эфиром в присутствии различных нитратов. [37]
 |
Особые виды изотерм обмена. [38] |
Изотермы обмена и кривые титрования не заменяют, а только дополняют друг друга. При изучении сорбции катионов, находящихся в малых количествах, часто определяют сорбцию катиона на фоне высокой и постоянной концентрации кислоты ( gn ж g и сн с) и результаты изображаются в виде зависимости логарифма коэффициента распределения от концентрации кислоты. Последний способ наиболее часто встречается в радиохимических исследованиях. [39]
 |
Зависимость коэффициента распределения необменно-поглощенного электролита от его концентрации во внешнем растворе. [40] |
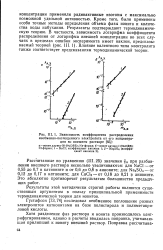
Кроме того, были применены особо точные методы определения объема фазы ионита и количества воды набухания. Результаты подтверждают термодинамическую теорию. В частности, зависимость логарифма коэффициента распределения от логарифма внешней концентрации во всех случаях в пределах ошибки эксперимента имеет наклон, предсказываемый теорией ( рис. III. Влияние валентного типа электролита также соответствует предсказаниям термодинамической теории. [41]
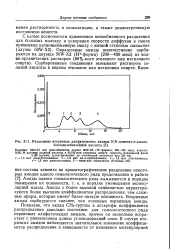 |
Разделение вторичных алифатических амидов N. N-диметил-га - амино-бензолазобензойной кислоты. [42] |
Амиды с более высокой основностью характеризуются более высоким коэффициентом распределения, чем сложные эфиры, которые имеют более низкую основность. Вторичные амиды сорбируются сильнее, чем основные первичные амиды. Показано, что вклад СНа-группы в логарифм коэффициента распределения довольно постоянен для гомологического ряда первичных алифатических амидов, причем он несколько возрастает с уменьшением длины углеводородной цепи. [43]
 |
Зависимость молекулярной сорбции и ионного обмена от равновесной концентрация на иодидной форме анионита дауэкс-1 х 2. [44] |
Закономерности, связанные с влиянием длины цепи на величину обмена и сорбции, можно особенно наглядно проследить по величинам коэффициентов распределения вещества в процессе обмена и сорбции при равновесной концентрации, стремящейся к нулю. Эти величины были найдены из начальных наклонов изотерм обмена и молекулярной сорбции. На рис. 4 и 5 приведены логарифмы коэффициентов распределения для обмена К0 и молекулярной сорбции Кс в зависимости от числа углеродных атомов в молекуле кислоты для анионитов дауэкс-1 X1 и дауэкс-1 X 2 в хлориднои форме. Видно, что величина молекулярной сорбции для кислот с числом атомов углерода более четырех растет с удлинением углеводородной цепочки молекулы кислоты более резко, чем для низших кислот. Правило Траубе, которое требует, чтобы вклад каждой СН2 - группы в работу сорбции или обмена был одинаковым, соблюдается для кислот от муравьиной до масляной включительно с меньшим коэффициентом, чем для кислот от валериановой и выше. [45]
Страницы: 1 2 3 4