Ацилхлорид
Cтраница 3
Аминолиз ангидридов кислот и ацилхлоридов обычно идет очень легко и является наиболее удобным способом получения амидов. Высвобождающийся хло-роводород ( или карбоновая кислота при ацилировании ангидридами) связывает эквимолярное количество амина, если не применять пиридина или других третичных аминов или щелочей для связывания кислоты. [31]
Единственным важным методом получения ацилхлоридов является реакция карбоновых кислот с хлоридами неметаллов ( разд. Можно использовать трихлорид или пентахлорид фосфора, однако тионилхлорид - наиболее удобен, поскольку сам реагент является летучим веществом и продукты реакции - газы. [32]
 |
Равновесие между альдегидами и 1 1-диолами в воде. [33] |
Кроме того, реакция ацилхлоридов со спиртами необратима, а реакция карбоновых иислот со спиртами обратима. Тем не менее вследствие того, что в последней реакции сложный эфир образуется прямо из карбоноеой кислоты, этот метод часто более удобен, так как не требуется дополнительной стадии синтеза ацилхлорида. [34]
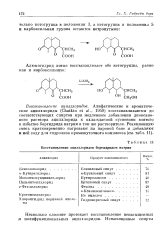 |
Восстановление ацилхлоридов боргидридом натрия. [35] |
Несколько сложнее протекает восстановление ненасыщенных и полифункциональных ацилхлоридов. [36]
Успешному ацилнровапню литиевых енолятов ацилхлоридам акция 16) способствуют низкие температуры. [37]
Успешному ацилнровапию литиевых енолятов ацилхлоридами акция 16) способствуют низкие температуры. [38]
Ацилирование свободных р-дикарбонильных соединений ацилхлоридами в пиридине также приводит к образованию О-ацилированных продуктов. Ацилирующим агентом в этом случае служит первоначально образующаяся соль ацилпириди-ння. [39]
Фриделя - Крафтса с ацилхлоридами ( разд. [40]
Успешному ацилнровапню литиевых енолятов ацилхлоридами ( реакция 16) способствуют низкие температуры. [41]
Самые реакционноспособные карбонильные соединения - ацилхлориды - могут еще взаимодействовать по Фриделю - Крафтсу в присутствии очень эффективного хлорида алюминия-с относительно инертными галогенобензолами, в то время как хлорметилирование формальдегидом в присутствии хлоро-водорода и хлорида цинка происходит лишь с ароматическими соединениями, имеющими реакционную способность, близкую к бензолу. Формилирование амидами кислот в присутствии РОСЬ по Вильсмейеру удается гладко только для полициклических углеводородов, фенолов и их эфиров, аминов. Наконец, очень инертный диоксид углерода реагирует без добавления электрофильного катализатора только с самыми реакционноспо-собными ароматическими соединениями - фенолятами. [42]
Как известно 14 48, ацилхлориды реагируют с ациклическими и циклическими простыми эфирами в присутствии большого количества катализатора ( ZnCl2, FeCl3) с образованием соотве-ствующих сложных эфиров. [43]
Альдегиды можно прямо превратить в ацилхлориды при обработке хлором; однако реакция происходит только с альдегидами, не содержащими а-водорода, и даже в этих случаях не всегда успешно. По-видимому, реакции идут по механизмам свободнорадикального типа. Под действием № - БС ( и УФ-облу-чения) [129] альдегиды превращают в ацилбромиды. [44]
Из ацилгалогенидов наиболее часто встречаются ацилхлориды, и их химические свойства типичны для функциональной группы в целом. [45]
Страницы: 1 2 3 4