Достижение - адсорбционное равновесие
Cтраница 1
Достижение адсорбционного равновесия при внутридиффу-зионном механизме массопереноса зависит от величины энергии взаимодействия системы адсорбат - адсорбент и ряда других факторов: размеров гранулы адсорбента, структуры зерна пористости, геометрии пор, соотношения между размерами молекул вещества и радиусами пор), концентрационных условий проведения процесса. [1]
Достижение адсорбционного равновесия зависит от парциального давления адсорбируемого газа, причем равновесие достигается тем быстрее, чем меньше парциальное давление. [2]
Быстрота достижения адсорбционного равновесия различна: так, при адсорбции СО2наугле оно наступает уже через 20 сек, при адсорбции О2 - через 2 5 час, при адсорбции N2 - через 20 час. Скорость адсорбции имеет большое значение для практического использования различных адсорбентов. Здесь необходимо указать, что активированный уголь в противогазе играет роль не только адсорбента ряда отравляющих веществ, но и катализалфа реакций разложения некоторых из них. [3]
Инсгда медленность достижения адсорбционного равновесия указывает на химическую реакцию, протекающую параллельно адсорбционному процессу. [4]
Запрограммировано время достижения адсорбционного равновесия. Для получения изотермы определяют несколько точек. [5]
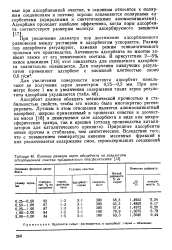 |
Влияние размера зерен адсорбента на результаты адсорбционной очистки туймазинского деасфальтизата. [6] |
При увеличении диаметра пор достижение адсорбционного равновесия между раствором и адсорбентом ускоряется. Размер пор адсорбента регулируют, изменяя режим технологического процесса его производства. Активность адсорбента во многом зависит также от его химического состава. В присутствии 2 - 5 % окиси алюминия [15] этот показатель для силикатного адсорбента значительно повышается. [7]
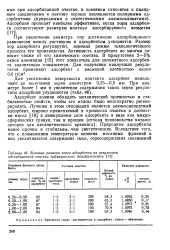 |
Влияние размера зерен адсорбента на результаты адсорбционной очистки туймазинского деасфальтизата. [8] |
При увеличении диаметра пор достижение адсорбционного равновесия между растворам и адсорбентом ускоряется. Размер пор адсорбента регулируют, изменяя режим технологического процесса его производства. Активность адсорбента во многом зависит также от его химического состава. В присутствии 2 - 5 % окиси алюминия [15] этот показатель для силикатного адсорбента значительно повышается. [9]
Ге - адсорбированное количество при достижении адсорбционного равновесия в растворе с концентрацией адсорбирующегося вещества с, Гоо - максимальная адсорбция ( при полном покрытии поверхности монослоем), Р - адсорбционная постоянная. [10]
Уменьшение размера зерен активного угля резко ускоряет достижение адсорбционного равновесия и соответственно сокращает длину зоны массообмена при фильтровании раствора ПАВ через слой активного угля, загруженного в адсорбционную колонну. [11]
С ростом температуры адсорбция уменьшается, но ускоряется достижение адсорбционного равновесия. [12]
Сопоставление газохроматографических данных, полученных при допущении о достижении адсорбционного равновесия, с данными, полученными статическими методами, показывает, что на однородных поверхностях в отсутствии предадсорбции или, хемосорбции оба метода дают близкие результаты. Особенно хорошие результаты получены для однородного непористого и неспецифического адсорбента - графитированной термической сажи J. Результаты, также близкие к статическим, получаются при использовании газохрома-тографического метода для изучения адсорбции относительно слабо адсорбирующихся благородных газов, низших углеводородов и не слишком сильно адсорбирующихся среднекипящих углеводородов ( при достаточно высоких температурах колонн) на геометрически весьма однородных пористых кристаллах цеолитов. Удовлетворительные результаты были получены также и для неоднородных поверхностей 8, худшие результаты получаются обычно для сравнительно сильно адсорбирующихся веществ на адсорбентах с неоднородной поверхностью. Так, было найдено 9, что полученные газо-хроматографическим методом в интервале температур колонн от 50 до 150 С теплоты адсорбции - алканов С6 - С8 и бензола на си-ликагелях с порами размером от 100 до 10 000 А на 15 - 20 % ниже измеренных в калориметре при тех же заполнениях той же поверхности. [13]
Уравнение показывает, что существует определенное соотношение ( после достижения адсорбционного равновесия) между количеством вещества, адсорбированным одним граммом адсорбента, и концентрацией того же вещества, оставшегося в растворе. [14]
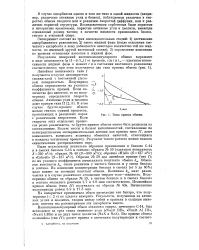 |
Типы кривых обмена. [15] |
Страницы: 1 2 3 4