Достижение - эквивалентная точка
Cтраница 1
Достижение эквивалентной точки в процессе титрования должно протекать с достаточной четкостью. [1]
После достижения эквивалентной точки кривая поднимается более круто из-за введения избытка ОН - - ионов. [3]
После достижения эквивалентной точки появление из - бытка ионов С и D - во всех случаях вызывает резкое увеличение электропроводности. [4]
После достижения эквивалентной точки, когда все ионы С1 - будут связаны, ионы Hg2 обнаруживаются при помощи индикатора - нитропруссида натрия или дифенилкарбазона, образующих с ионами Hg2 осадок синего цвета. [5]
Поэтому достижение эквивалентной точки сопровождается переходом окраски раствора от вишнево-красной к синей. [6]
После достижения эквивалентной точки, когда все ионы С1 - будут связаны, ионы Hg2 обнаруживаются при помощи индикатора-ни-тропруссида натрия или дифенилкарбазона, образующих с ионами Hg2 осадок синего цвета. [7]
После достижения эквивалентной точки избыток титранта гидролизуется и дает сильно щелочную - среду, что фиксируется с помощью кислотно-основного индикатора фенолфталеина. [8]
При достижении эквивалентной точки концентрация определяемого иона в растворе резко снизится, вследствие чего резко изменится потенциал электрода. [9]
В момент достижения эквивалентной точки, когда весь катион будет связан комплексоном, в растворе возникает окраска свободного индикатора, отличающаяся от окраски комплексного соединения этого индикатора с катионом. [10]
 |
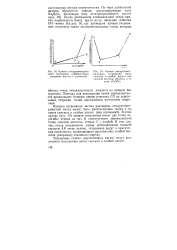
Схема полярографической установки.| Полярограмма раствора, содержащего несколько ионов. [11] |
Избыточная капля после достижения эквивалентной точки вызывает дальнейшее, но уже значительно меньшее увеличение отсчета на шкале милливольтметра. [12]
Опалесценция указывает на достижение эквивалентной точки титрования. Если в растворе присутствует свободная синильная кислота, то он мутнеет после первой же капли раствора AgN03 вследствие образования нерастворимого в воде цианида серебра. Поэтому свободная HCN должна быть предварительно нейтрализована гидроокисью натрия. В качестве индикатора в этом анализе используют иодид калия. Применение его имеет то преимущество, что иодид серебра, нерастворимый в растворах NaOH, легко растворим в щелочном цианиде. Он осаждается из раствора раньше цианида серебра, что позволяет установить конец титрования более точно. [13]
И только по достижении эквивалентной точки, когда в анализируемом растворе появится избыток ионов титранта, восстанавливающихся ( или окисляющихся) на электроде, повышается сила тока. [14]
Вблизи или сразу после достижения эквивалентной точки по сероводороду частицы сернистого серебра быстро укрупняются, раствор делается прозрачным. [15]
Страницы: 1 2 3 4