Аминотрансфераза
Cтраница 2
Реакции переаминирования катализируются специфическими аминотрансферазами, относящимися к группе пири-доксалевых ферментов. [16]
Фосфопиридоксаль входит в состав аминотрансфераз, катализирующих перенос аминогрупп ряда аминокислот ( гл. Кроме того, идентифицировано более 50 пиридоксальфосфатных ферментов, катализирующих разнообразные реакции, такие, как декарбоксилирование аминокислот, рацемизация, дегидротирование, гидролитическое расщепление субстратов. Фосфопиридоксалевые ферменты катализируют синтез сфингозина, а также реакции р-замещения. [17]
В настоящее время определение аминотрансфераз в сыворотке крови приобретает важное диагностическое значение. В норме содержание аминотрансфераз в сыворотке крови незначительно, а в тканях, например в мышце сердца, в ткани печени, скелетных мышцах и других относительно велико. [18]
Процесс переаминирования катализируется ферментами аминотрансферазами ( трансаминазами), у которых коферментом служит производное витамина Be - фосфо-пиридоксаль. [19]
Чем отличаются методы оценки активности аминотрансфераз средствами сухой и влажной химии. [20]
В противоположность аминотрансферазам животных тканей и микроорганизмов растительные аминотрансферазы продолжают оставаться недостаточно четко охарактеризованной группой, в частности это относится к их специфичности в отношении амино - и кетокислот. Подобный вывод был сделан в отношении аминотрансферазы из проростков маша, поскольку скорости переаминирования различных аминокислот с а-кетоглутаратом были в данном случае аддитивными; если бы все реакции переаминирования катализировались одним ферментом, то конкуренция между аминокислотами за доступные молекулы фермента приводила бы к взаимному ингибирующему действию. Однако решающие доказательства довольно высокой специфичности растительных аминотрансфераз были получены в немногочисленных исследованиях, проведенных с очищенными ферментами. Аспартат-глутамат - аминотрансфераза из головок цветной капусты была очищена более чем в 20Q раз [23], причем оказалось, что фермент обладает довольно высокой субстратной специфичностью. При использовании оксалоацетата в качестве акцептора аминогруппы помимо глутамата в какой-то степени активными донорами аминогруппы были только цистеиновая и цистеинсульфиновая кислоты. Эти серусодержащие аминокислоты, напоминающие глутаминовую кислоту тем, что они содержат вторую карбоксильную группу у р-углеродного атома, реагируют примерно в 4 раза слабее, чем нормальный субстрат. [21]
В этих же условиях незначительное снижение активности аминотрансфераз к концу 60-дневного эксперимента прогрессирует, становясь статистически выявляемым. Между тем ослабление активности кетозо-1 - фосфатальдолазы обнаруживается на 60 - й и 90 - й день опыта. [22]
АСПАРТАТАМИНОТРАНСФЕРАЗА ( Ь - аспартат: 2-оксо-глутарат аминотрансфераза), фермент класса трансфераз, катализирующий при участии кофермента пиридоксаль-5 - фосфата обратимый перенос аминогруппы ( трансаминиро-вание) от Ь - аспарагиновой к-ты ( ф-ла I) на 2-оксоглутаро-вую ( II) с образованием щавелевоуксусной ( III) н Ь - глута-миновой ( IV) к-т. [23]
Применяются дополнительные лабораторные тесты: определение уровня сывороточных аминотрансфераз и количества глобулинов. [24]
В реакциях переаминирова-ния, катализируемых трансаминазами, или аминотрансферазами, прочно связанный пиридоксальфосфат служит промежуточным переносчиком аминогруппы от ее донора - ос-аминокислоты-к акцептору - ос-кетокислоте. В процессе каталитического цикла тран-саминаз аминогруппа вступающей в реакцию аминокислоты сначала переносится на связанный с ферментом пиридоксальфосфат. Образовавшееся при этом аминопроизводное кофермента-пиридоксаминфосфат-передает затем аминогруппу второму субстрату - ос-ке-токислоте и возвращается в исходную пиридоксальфосфатную форму. В подобных реакциях переаминирования могут участвовать самые разнообразные аминокислоты и а-кетоглутарат, который играет роль универсального акцептора аминогрупп и в ходе реакции превращается в глутаминовую кислоту-ключевой продукт метаболизма аминогрупп. [25]
В соответствии с давно принятым постулатом в активном центре пиридоксальфосфат-зависимых ферментов, таких, как аминотрансферазы ( трансаминазы), конъюгат аминокислоты с пиридоксальфосфатом ориентирован таким образом, чтобы связь с а-водородным атомом располагалась почти перпендикулярно плоскости пиридинового цикла. [27]
Алании образуется в реакции переамннированля из пирувата ( см. § 4.2) с участием аланин аминотрансферазы. [28]
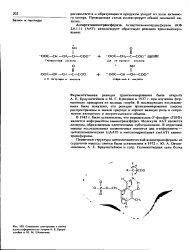 |
Смешение электронов к атому азота кофермента по теории А. Е. Браун-штейна и М. М. Шемякина. [29] |
В 1945 г. было установлено, что пиридоксаль-5 - фосфат ( ПЛФ) является коферментом аминотрансфераз. Молекула ААТ является димером, образованным идентичными субъединицами. В сердечной мышце исследованных позвоночных имеются два изофермента - цитоплазматическая ( цААТ) и митохондрнальная ( мААТ) а ми но-трансферазы. [30]
Страницы: 1 2 3 4
