Метод - валентная связь
Cтраница 1
Метод валентных связей ( локализованных электронных пар) строится на положении о том, что каждая пара атомов в молекуле удерживается вместе при помощи одной или нескольких общих электронных пар. [1]
Метод валентных связей не позволяет объяснить состав, строение и свойства всего многообразия комплексных соединений. Значительно шире используются теории кристаллического поля и молекулярных орбиталей. [2]
Метод валентных связей был первой квантовомеханической теорией химической связи, основанной на химическом толковании связи как образования, прочность которого зависит от наличия двух спаренных электронов. Эта теория концентрирует внимание на спаренных электронах молекулы ( приближение идеального спаривания) и исходит из предположения, что они играют основную роль в образовании связи. [3]
Метод валентных связей, который часто называют также методом локализованных пар, ведет свое прямое происхождение от упомянутых в предыдущей главе работ Гейтлера, Лондона, Слей-тера и Полннга. [4]
Метод валентных связей более нагляден и удобен для качественного рассмотрения химической связи. На его основе рассматривается понятие о гибридизации орбиталей. Атомы, входящие в молекулу, рассматриваются как индивидуальные частицы, а связи - результат взаимодействия валентных электронов в атоме. Метод молекулярных орбиталей дает более точное количественное представление о состоянии электронов в молекуле. С его помощью возможно описание более тонких квантово-меха-нических эффектов в биофизике и биохимии. Он лучше приспособлен для объяснения спектров молекул и теоретических пространственных расчетов. В настоящее время он более популярен, особенно ввиду применения мощных вычислительных машин. [5]
Метод валентных связей ( ВС) широко используетсл химиками. В рамках этого метода большая и сложная молекула рассматривается как состоящая из отдельных двухцентровых и двух-электронных связей. Принимается, что электроны, обусловливающие химическую связь, локализованы ( расположены) между двумя атомами. К большинству молекул метод валентных связей может быть применен с успехом. Однако имеется ряд молекул, к которым этот мето71 неприменим или его выводы находятся в противоречии с опытом. [6]
Метод валентных связей и метод молекулярных орбиталей отличаются друг от друга выбором пробной волновой функции. [7]
Метод валентных связей указывает на возможность существования борина ВНз, однако это соединение не может быть выделено и существует только как промежуточный йродукт в некоторых химических реакциях. [8]
Метод валентных связей ( МВС) широко используется химиками. В рамках этого метода большая и сложная молекула рассматривается как состоящая из отдельных двухцентровых и двух-электронных связей. Принимается, что электроны, обусловливающие химическую связь, локализованы ( расположены) между двумя атомами. К большинству молекул метод валентных связей может быть применен с успехом. Однако имеется ряд молекул, к которым этот метод неприменим или его выводы находятся в противоречии с опытом. [9]
Метод валентных связей фиксирует этот опытный факт с помощью гипотетического механизма гибридизации. [10]
Метод валентных связей является развитием подхода, к-рый был применен в 1927 Гайтлером и Лондоном к первому квантово-механич. Существуют две простые волновые функции, пригодные для описания такой системы и удовлетворяющие требованию симметрии квадрата волновой функции, вытекающему из физич. [11]
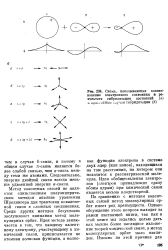 |
Схема. показывающая возникновение электронного состояния в результате гибридизации состояний ( а. [12] |
Метод валентных связей не является единственным полуэмпирическим методом анализа уравнения Шредингера для трактовки ковалент-ной связи в сложных соединениях. Среди других методов безусловно заслуживает внимания метод молекулярных орбит. [13]
Метод валентных связей будет рассмотрен первым, так как по основным положениям он наиболее простой и прекрасно служит в течение более четверти века для объяснения некоторых свойств комплексов. Даже сейчас, когда недостатки этого метода ясно видны, большое число химиков все еще находит его удобным для интерпретации и сопоставления своих результатов. Затем мы об судим электростатическую теорию, особенно обращая внимание на теорию кристаллического поля. Эта последняя оказалась са мой удачной из трех для удовлетворительного сопоставления свой ств комплексов, а также по числу вычислений и предсказаний, которые она позволяет сделать. Наконец, мы кратко обсудим ме год молекулярных орбиталей. [14]
Метод валентных связей предсказывает неэквивалентность длин связей в нафталине: в двух из трех возможных резонансных форм связь C ( D - С2 - j ная и в одной - одинарная, в то время как связь С) - С ( з - двойная: зонансных формах и одинарная в одной. Статистически можно предположить, что первая связь представляет 0 67 долей от двойной связи, а вторая - 0 33 доли. [15]
Страницы: 1 2 3 4