Метод - валентная связь
Cтраница 2
Метод валентных связей постепенно заменяется методом молекулярных орбиталей, который становится ведущим методом теоретического исследования строения молекул во многих областях химии, в частности в органической химии. Однако использование-метода МО даже в его простейшей форме ЛКАО ( линейной комбинации атомных орбиталей) для трактовки природы молекул неорганических соединений еще только начинает приобретать всеобъемлющее значение как в научных исследованиях, так и в педагогической практике. Все сказанное делает понятным огромный интерес химиков, в особенности химиков-педагогов, к современным воззрениям в неорганической химии. К сожалению, очень мало руководств или монографий на русском языке, излагающих новейшие теоретические представления о природе строения неорганических молекул и описывающих пути развития современной неорганической химии. [16]
Метод валентных связей ( ВС) представляет собой другой, отличный от метода МО, способ описания делокализации электронов при образовании химической связи. При этом делокализация электронов описывается как своего рода обмен, который приводит к тому, что в пространстве между атомами возникает повышенная электронная плотность, обеспечивающая их связь. В соответствии с принципом Паули два обменивающихся электрона, образующие связывающую пару, должны иметь противоположные спины. [17]
Метод валентных связей указывает на возможность существования боро-водорода ВНз, однако это соединение не может быть выделено и существует только как промежуточный продукт в некоторых химических реакциях. Молекула ВНз неустойчива ( АС. [18]
Метод валентных связей очень нагляден и поэтому удобен для качественного обсуждения многих экспериментальных данных. Поэтому химики-органики продолжают им широко пользоваться. [19]
Метод валентных связей ( ВС) разработан Гейтлером и Лондоном ( 1927) Г при изучении строения молекулы водорода. [20]
Метод валентных связей ( ВС) предложен Гейтле-ром и Лондоном ( 1927) при изучении строения молекулы водорода. Метод основан на предположении, что связь между атомами образуется парой электронов в процессе сближения и взаимодействия атомов. Допускается, что наиболее существенные свойства образующейся молекулы ( значения энергии, распределение электронного облака) могут быть выражены не какой-нибудь одной валентной схемой, а совокупностью небольшого их числа, построенных с учетом опытных данных. Например, молекула водорода может быть изображена тремя валентными структурами Нв - Hj, НГ - Н и На - НгГ с различным расположением ( смещением) электронной пары. [21]
 |
Энергетические уровни атомов ванадия, ниобия и тантала. [22] |
Метод валентных связей исходит из того, что в образовании химической связи участвуют либо только неспаренные электроны атомов, либо свободные орбитали одного атома и электронная пара другого. В методе молекулярных орбиталей считается, что все электроны атомов участвуют в образовании молекулярных орбиталей. Метод молекулярных орбиталей менее наглядный, но более строгий, чем метод ( валентных связей. [23]
 |
Ионные радиусы некоторых элементов. [24] |
Метод валентных связей основывается на предположении, что химическая связь в основном определяется двухэлектрон-ной связью. В комплексных соединениях эта связь осуществляется электронами, расположенными на различных энергетических уровнях иона-комплексообразователя. Поэтому даже в соединениях с одинаковыми лигандами ( молекулами или ионами, непосредственно связанными с центральным атомом - комплексообразователем) прочность химических связей различна. Так, связь, образованная s - электронами, плотность которых имеет сферическую симметрию, отличается по прочности от связи, образованной р-электронами. В то же время результаты экспериментов показывают, что одинаковые лиганды могут образовывать с комплексообразователем близкие по прочности и структуре связи. [25]
Метод валентных связей ( ВС) возник непосредственно на базе расчета молекулы водорода, выполненного Гайтлером и Лондоном ( разд. Основная физическая идея метода ВС базируется на том представлении, что химическая связь образуется в результате спаривания спинов двух электронов, находящихся на однократно занятых валентных орби-талях соответствующих атомов молекулы; основная цель метода ВС состоит в построении соответствующих электронных молекулярных волновых функций, для которых возможные химические связи описываются как результат спаривания отдельных пар электронов. Эту процедуру построения многоэлектронной волновой функции в методе ВС мы уже сопоставляли ( разд. МО, основная задача которого - добиться представления волновой функции одним детерминантом, в котором молекулярные орбитали, каким-либо образом делокализованные по всей молекуле, являются линейными комбинациями рассматриваемых базисных атомных орбиталей АО. Метод ВС как метод построения достаточно хороших молекулярных электронных волновых функций сильно дискредитировали за последние двадцать лет, и теперь его обычно рассматривают просто как некоторую полуэмпирическую схему, в которой многие величины считаются эмпирическими параметрами. Вместе с тем следует подчеркнуть, что на основе метода ВС можно развить математически совершенно строгую теорию, которую с успехом можно использовать для проведения неэмпирических расчетов. Метод ВС заслуживает большего внимания, чем обычно ему уделяют. [26]
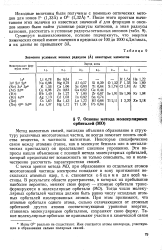 |
Значения условных ионных радиусов ( А некоторых элементов. [27] |
Метод валентных связей, наглядно объясняя образование и структуру различных многоатомных частиц, не всегда помогает понять свойства вещества, в частности магнитные. Некоторые специфические связи между атомами ( такие, как в молекуле бензола или в металлических кристаллах) он представляет слишком упрощенно. Эти вопросы нашли объяснение с позиций метода молекулярных орбиталей, который предоставляет возможность не только описывать, но и количественно рассчитать характеристики связей. [28]
Метод валентных связей ( локализованных электронных пар) исходит из положения, что каждая пара атомов в молекуле удерживается вместе при помощи одной или нескольких общих электронных пар. [29]
Метод валентных связей дает теоретическое обоснование широко применяемым химиками структурным формулам. Большое достоинство метода заключается в его наглядности. Однако представление о локализованных ( двухцентровых, двухэлектронных) химических связях оказывается слишком узким для объяснения многих экспериментальных фактов. В частности, метод валентных связей несостоятелен для описания молекул с нечетным числом электронов, большой группы молекул с дефицитом электронов, свойств соединений, синтезированных в последнее время. Большие трудности испытывает этот метод при объяснении магнитных свойств соединений, их окраски, энергетических характеристик молекул и многих других важных экспериментальных фактов. [30]
Страницы: 1 2 3 4