Метод - переходное состояние
Cтраница 1
Метод переходного состояния в принципе может быть применен в рамках любого метода расчета волновых функций для определения энергии ионизации уровня. [1]
Метод переходного состояния позволяет с помощью уравнений, приведенных выше, рассчитывать разные величины, входящие в выражение скорости реакции на поверхности. Такие расчеты могут сводиться к следующему. [2]
Применение метода переходного состояния значительно расширило возможности теоретического подхода к решению кинетических задач. К числу результатов, которые могут быть получены при помощи этого метода ( без знания потенциальных поверхностей, определяющих течение элементарных актов), относится, в частности, зависимость константы скорости химической реакции от давления. [3]
Применение метода переходного состояния значительно расширило возможности теоретического подхода к решению кинетических задач. Однако современное состояние теории этого метода представляется крайне неудовлетворительным. Многие выводы теории абсолютных скоростей реакций, в особенности расчеты энергий активации, не верны и нуждаются в серьезном пересмотре. [4]
Применение метода переходного состояния позволяет для большинства исследованных реакций решить качественно, а в некоторых случаях и количественно вопрос о влиянии давления на их скорость. Решение указанной задачи производится методами термодинамики и статистической механики без введений дополнительных допущений или гипотез. [5]
Основу метода переходного состояния представляет понятие об активированном комплексе, образование и разложение которого является необходимым условием осуществления каждого элементарного акта ( см. гл. [6]
Пользуясь методом переходного состояния, нетрудно оценить пред-экспоненциальный множитель в уравнении Аррениуса для скорости водородного обмена в трехмо лекулярном комплексе. [7]
Чтобы применять метод переходного состояния к реакциям с участием заряженных или полярных частиц, необходимо знать зависимость коэффициентов активности этих частиц от условий эксперимента. Электростатические взаимодействия проявляются на большом расстоянии; на заряженные частицы в растворе влияют не только ближайшие соседние частицы, но и ионы и молекулы, находящиеся на довольно значительном расстоянии. [8]
В основе метода переходного состояния лежит предположение, что протекание реакции не нарушает существенно распределения молекул по состояниям, так что оно отвечает статистически равновесному Максвелл-Больцмановскому распределению. Область применимости этого предположения совпадает с областью применимости закона действующих масс и уравнения Аррениуса. [9]
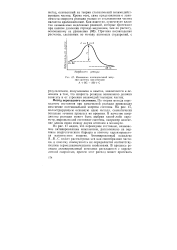 |
Изменение потенциальной энергии системы при реакции A - f ВС - АВ С. [10] |
По теории метода переходного состояния при химической реакции происходит изменение потенциальной энергии системы. На рис. 47, иллюстрирующем основную идею метода, схематически показано течение процесса во времени. В качестве координаты реакции может быть выбран какой-либо параметр, выражающий состояние системы, например изменение длины связи между двумя атомами в молекуле. [11]
Основное положение метода переходного состояния, которое не является строго доказанным, утверждает, что во время реакции существует равновесие между исходными веществами и активированными комплексами. Из этого положения и выводится основное уравнение метода переходного состояния. [12]
Рассмотрим применение метода переходного состояния в общем виде к некоторым типам реакций. [13]
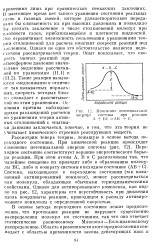 |
Изменение потенциальной. [14] |
В основе метода переходного состояния лежит предположение, что протекание реакции не нарушает существенно распределения молекул по состояниям, так что оно отвечает статистически равновесному Максвелл-Больцмановскому распределению. [15]
Страницы: 1 2 3 4