Метод - переходное состояние
Cтраница 2
 |
Примеры наложений активированного комплекса на поверхности для разных граней кристаллической решетки никеля. ( ПО. g - 2. ( 100. g4. ( 111. g6. [16] |
При распространении метода переходного состояния на каталитические процессы возникают осложнения. Поэтому каждая стадия сложного процесса должна рассматриваться отдельно. [17]
На основе метода переходного состояния автором был разработан и применен приближенный метод расчета стерических факторов радикальных реакций. [18]
Обычный вариант метода переходного состояния устанавливает корреляцию между / и f допущением, что пересечение 5 обязательно ведет к завершению реакции. [19]
 |
Изменение потенциальной энергии системы при реакции А BG АВ С. [20] |
В теории метода переходного состояния делается предположение, что всегда существует равновесие между молекулами в исходном состоянии и активированными комплексами. Это предположение теоретически не обосновано и представляет собой наиболее спорный тезис рассматриваемой теории. Оно, однако, пока необходимо для вывода основного ее уравнения. [21]
Общие принципы метода переходного состояния сохраняются при распространении его на процессы с участием твердых поверхностей, хотя и возникают осложнения, связанные с конфигурацией активированных комплексов и выделением элементарных реакций. Поверхность твердого тела - катализатора или адсорбента ( топохимические реакции мы здесь опускаем) - должна рассматриваться как место локализации активированных комплексов, в состав которых в качестве равноправных компонентов и входят участки этой поверхности. [22]
 |
Фазовое пространство системы, переходники из начального состояния / в конечное состояние II черед элемент dT критической поверхности S но фазовой траектории L. [23] |
Таким образом, метод переходного состояния представляет практическую ценность только в тех случаях, когда неизбежный произвол в выборе модели активированного комплекса и неопределенность величины % не сильно влияют на конечный результат. [24]
Третий член отличает метод переходного состояния от метода энергии локализации. Этот член как при очень больших, так и при очень малых ( Ьг L2) должен приводить к отклонениям от правила Поляни в сторону меньших значений энергии активации. Оценки величины ( Lv L2 - 2) la показывают, что третий член в ( 15) во всех реальных случаях не имеет значения. [25]
Таким образом, метод переходного состояния представляет практическую ценность только в тех случаях, когда неизбежный произвол в выборе модели активированного комплекса и неопределенность величины % не сильно влияют на конечный результат. [26]
Таким образом, метод переходного состояния вскрывает также смысл констант скорости адсорбции и десорбции для процессов, описываемых законом действующих поверхностей. [27]
Таким образом, метод переходного состояния позволяет получить выражения скоростей разных элементарных стадий поверхностных реакций. После работы [108] рассмотрение этих вопро-сов ( хотя и менее строгое) было проведено Глесстоном, Лейдле-ром и Эйрингом [154] и затем оно было распространено также и на электродные процессы. [28]
Несмотря на недостатки метода переходного состояния, в ряде случаев он оказывается весьма полезен, поскольку дает простейшую интерпретацию константы & реакц через динамические характеристики исходных молекул, активированного комплекса и высоту Еа потенциального барьера. [29]
 |
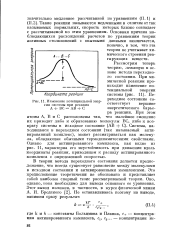
Зависимость константы скорости присоединения радикалов от величины A. Ei2 согласно уравнению ( 12. [30] |
Страницы: 1 2 3 4