Метод - переходное состояние
Cтраница 4
Здесь мы кратко напомним основные предпосылки метода переходного состояния [7, 9, 26, 27, 118, 137, 648], с помощью которого дается современная трактовка смысла величин констант скорости. [46]
В литературе имеются работы, где методом переходного состояния рассчитывались значения трансмиссионных коэффициентов к для суждения об адиабатичности или неадиабатичности рассматриваемых реакций. В работе [183] для реакции гидрирования окиси углерода на никеле вычисленные и экспериментально найденные величины энтропии активации резко различались. [47]
Лучше всего в этом убедиться, применяя метод переходного состояния к рассмотрению влияния изотопного замещения на скорость реакции АН В А НВ, точно так же, как это было сделано в формулах ( 131) ( 137) для термодинамического изотопного эффекта. В данном случае хорошей аппроксимацией координаты реакции х может служить положение протона между двумя центрами - А и В. [48]
Рассмотрим теперь теорию, лежащую в основе метода переходного состояния. Переходное состояние соответствует вершине энергетического барьера реакции. Система, находящаяся в переходном состоянии ( так называемый активированный комплекс), может рассматриваться как молекула, обладающая обычными термодинамическими свойствами. Однако для активированного комплекса, как видно из рис. 18, характерна его неустойчивость при движении вдоль координаты реакции, приводящем к распаду активированного комплекса с определенной скоростью. [49]
Рассмотрим теперь теорию, лежащую в основе метода переходного состояния. Переходное состояние соответствует вершине энергетического барьера реакции. Система, находящаяся в переходном состоянии ( так называемый активированный комплекс), может рассматриваться как молекула, обладающая обычными термодинамическими свойствами. Однако для активированного комплекса, как видно из рис. 12, характерна его неустойчивость при движении вдоль координаты реакции, приводящем к распаду активированного комплекса с определенной скоростью. [50]
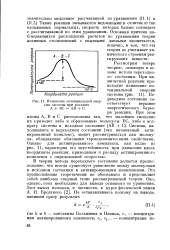 |
Изменение потенциальной энергии системы при реакции А BG АВ С. [51] |
Рассмотрим теперь теорию, лежащую в основе метода переходного состояния. Переходное состояние соответствует вершине энергетического барьера реакции. Система, находящаяся в переходном состоянии ( так называемый активированный комплекс), может рассматриваться как молекула, обладающая обычными термодинамическими свойствами. Однако для активированного комплекса, как видно из рис. 11, характерна его неустойчивость при движении вдоль координаты реакции, приводящем к распаду активированного комплекса с определенной скоростью. [52]
Уравнение (111.25) отличается от выражения, получаемого методом переходного состояния. [53]
Возможность нахождения статистических сумм и позволяет воспользоваться методом переходного состояния для расчетов предэкспоненциальных множителей констант скоростей реакций. [54]
Из изложенного вытекают пути расчетов абсолютных скоростей реакций методом переходного состояния. Эти расчеты сводятся к вычислению величин предэкспоненциальных множителей константы скорости соответствующей элементарной реакции. Величины энергии активации в принципе доступны квантовохимической оценке, и подобные расчеты могут рассматриваться как другая сторона приложения теории абсолютных скоростей реакций. [55]
Страницы: 1 2 3 4