Микомицин
Cтраница 1
Микомицин сильно вращает плоскость поляризации влево: [ CX ] D - 130; его брутто-формула С НюОг. При каталитическом гидрировании 1 01 ммоль вещества ( 200 мг) поглощалось 7 8 ммоль водорода и Получалась w - тридекановая кислота СН3 ( СН2) цСООН, Учитывая чрезвычайную неустойчивость микомицина, Селмер и Соломоне предприняли попытку выделить и охарактеризовать какой-либо более устойчивый продукт его превращения. Они нашли, что при действии избытка едкого натра на микомицин уже через несколько минут выпадает кристаллическая соль изомерной кислоты - изомикоми-цина. Этот изомер также поглощает 8 моль водорода при каталитическом гидрировании, давая н-тридекановую кислоту, и, следовательно, содержит ту же углеродную цепь из тринадцати атомов углерода, что и исходный микомицин. Однако изомикомицин оптически неактивен. Из определения С-метильных групп по методу Куна - Рота следует, что в микомицине таковых нет, в то время как в изомикомицине имеется одна СНз-группа. Принимая во внимание неразветвленный характер молекул обоих соединений, можно было сделать вывод, что метальная группа в изомикомицине занимает концевое ( Ci3) положение. В инфракрасных спектрах обоих изомерных соединений имеется полоса поглощения 1730 еж 1, характерная для карбоксильной группы, не сопряженной с двойной связью, из чего вытекает, что оба соединения содержат группировку - СН2 - СООН. В противоположность микомицину, изомикомицин очень легко реагирует с малеиновым ангидридом, давая дильс-альдеровский аддукт. Эта реакция свидетельствует о присутствии в изомикомицине сопряженной диеновой системы С С-С С, так как присоединение к ениновой системе СС-СС еновой компоненты должно было бы приводить к чрезвычайно напряженному циклу с алленовой системой связей. [1]
Микомицин активен в отношении грамположительных и грамотрица-тельных бактерий; он сильно подавляет in vitro Mycobacteriutn tuberculosis. Его активность не изменяется заметным образом в присутствии крови. Имеются указания, что микомицин не токсичен для мышей. [2]
Спектр микомицина можно было бы представить как наложение поглощения ендиина ( XLIII) и триена ( XLIV), поскольку двойные связи ал лена находятся в перпендикулярных плоскостях и фактически изолируют эти два хромофора. Карбоксильная группа отделена он ненасыщенных систем и не вносит никакого вклада в спектр. [3]
Оптическая активность микомицина обусловлена наличием алленовой группировки. [4]
И в микомицине, и в его изомере была доказана 3 5-диено-вая система, причем на основании данных ИК-спектров для микомици-на установлена З - транс-5 - ыс-конфигурация, а для изомикомицина - З - гранс-б - Гусанс-конфигурация. Как известно, транс-транс-лиепы намного легче вступают в диеновую конденсацию, чем тужнс - ыс-изомеры, однако несг особность микомицина реагировать с малеиновым ангидридом не может служить доказательством его конфигурации, поскольку сам антибиотик чрезвычайно неустойчив. [5]
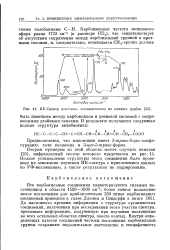 |
ИК-Спектр немотина, полиацетилена из низших грибов. [6] |
Предполагается, что микомицин имеет З - транс-5 - цис-ков. [7]
Аналогично изомеризуется и природный микомицин. [8]
Самой необычной ненасыщенной кислотой является микомицин, оптически активный антибиотик, продуцируемый микроорганизмом Norcardia acidophilis. [9]
Следующие данные свидетельствуют в пользу приведенных выше структур: микомицин дает осадок с AgNO3, что характерно для алкина-1; гидрирование с образованием тридекановой кислоты свидетельствует о том, что вещество представляет собой ненасыщенную кислоту с неразветвленной цепью. ИК-спектр микомицина указывает на наличие групп НСС -, ССС, СС-СС иСО; в таком случае оптическая активность микомицина должна быть обусловлена кумулированными двойными связями. Изомикомицин, согласно его ИК-спектру, не имеет кумулированных двойных связей; он не является алкином-1, но содержит структурное звено СН3 - СС -, поскольку окисление СгО3 дает уксусную кислоту, а так как он поглощает в более длинноволновой области, чем микомицин, он является более сопряженным по сравнению с последним. Для того чтобы давать аддукт Дильса - Альдера с малеиновым ангидридом, он должен иметь группировку СС-СС. [10]
Чрезвычайно неустойчивым соединением ( разлагающимся со взрывом при 75) является антибиотик микомицин, образуемый актиномицеюм fiiciardia acido-philus. [11]
Чрезвычайно неустойчивым соединением ( разлагающимся со взрывом при 75) является антибиотик микомицин, образуемый актиномицетом Nocardia acido-philus. [12]
Весьма примечательно, что кислая фракция экстракта из этого вида гриба содержала микомицин. [13]
 |
Некоторые полиацетиленовые антибиотики природного происхождения. [14] |
Наиболее изученными полиацетиленовыми антибиотиками, образуемыми микроорганизмами, являются агроцибин, биформин, диатретин-2, микомицин, немотин и немотйновая кислота, одиссии и одиссовая кислота. Перечисленные соединения также обладают сильным антибиотическим действием на различные виды бактерий и грибов. [15]
Страницы: 1 2 3 4