Ионная молекула
Cтраница 1
Ионные молекулы могут при известных условиях распадаться на ионы, из которых они получаются. Это распадание молекул на ионы называется диссоциацией. Если диссоциация происходит под влиянием высокой температуры, то такая диссоциация называется термической. [1]
Ионные молекулы при известных условиях распадаются на образующие их ионы. Этот процесс называется диссоциацией. [2]
Ионные молекулы состоят из противоположно заряженных ионов. [3]
Ионные молекулы существуют в веществах, находящихся в газообразном состоянии. При охлаждении они образуют геометрически правильные структуры, составляющие основу кристалла. [4]
 |
Схема и модель кристаллической решетки хлорида натрия. [5] |
Ионные молекулы существуют в веществах, находящихся в газообразном состоянии. При охлаждении они образуют геометрически правильные структуры, составляющие основу кристалла. Из кристалла невозможно выделить отдельные молекулы. Поэтому когда применяют к подобным кристаллическим ионным соединениям, слово молекула, то это допускается условно, чтобы показать состав и количественное соотношение ионов в соединении. [6]
Ионные молекулы являются объектами, с которыми химику приходится встречаться несравненно реже, чем с частицами, где атомы связаны ковалентной связью. [7]
Поэтому ионные молекулы в основном состоянии всегда диссоциируют на атомы, а не на ионы. [8]
Когда ионные молекулы поглощают свет в момент наибольшего сближения ядер, то, как видно из рисунка, небольшие вариации в значении г ведут к значительному изменению длины стрелок. Поэтому вместо узких полосок в спектре получаются целые области абсорбции, которые отвечают различным степеням возбуждения продуктов распада молекул. Потенциальные кривые молекул с атомной и ионной связью, а также их спектры поглощения сильно отличаются, поэтому изучение спектров и характера потенциальных кривых позволяет устанавливать тип химической связи. Такого рода исследования показали, например, что молекулы галогеноводородных кислот НС1, HBr, HI, a также галогениды таллия и серебра в газообразном состоянии являются не ионными, а атомными. [9]
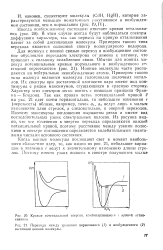 |
Кривые потенциальной энергии, комбинирующиеся г кривой отталкивания.| Переходы между уровнями нормального ( / и возбужденного ( 2 состояний ионной молекулы. [10] |
Когда ионные молекулы поглощают свет в момент наибольшего сближении ядер, то, как видно из рис. 21, небольшие вариации в значении г ведут к значительному изменению длины стрелок. [11]
Поэтому ионные молекулы в основном состоянии всегда диссоциируют на атомы, а не на ионы. [12]
 |
Термохимические циклы для расчета. [13] |
Поэтому ионные молекулы в основном состоянии всегда диссоциируют на атомы, а не на ионы. [14]
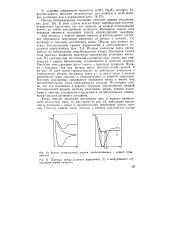 |
Кривые потенциальной энергии, комбинирующиеся с кривой оттал кивания.| Переходы между уровнями нормального ( / и возбужденного ( 2 состояний ионной молекулы. [15] |
Страницы: 1 2 3 4 5