Ионная молекула
Cтраница 4
Большой класс молекул образуют ионные молекулы, состоящие из ионов химических элементов, входящих в молекулу. Общая сумма положительных и отрицательных зарядов ионов в молекуле равна нулю, вследствие чего ионные молекулы электрически нейтральны. [46]
Как показано, возбуждение ионной молекулы приводит к переходу электрона от аниона к катиону, следовательно, распад такой возбужденной молекулы приведет к образованию нейтральных атомов. [47]
 |
Влияние органических. [48] |
Следовательно, в случае ионных молекул пробы гидрофобность и эффекты заряженности оказывают влияние на коэффициент распределения. [49]
В гетерополярных, или ионных молекулах электроны можно разделить на группы, каждая из которых совершает движение в основном около одного из ядер. При этом вблизи одного ядра располагается больше электронов, чем у исходного нейтрального атома, а вблизи другого - меньше. Тем самым вступившие во взаимодействие атомы превращаются как бы в разноименно заряженные ионы, между которыми возникают силы кулоновского притяжения, обеспечивающие устойчивое существование молекулы. [50]
Для твердых веществ, образуемых ионными молекулами, типичной является ионная структура, которая характеризуется наличием в узлах пространственной кристаллической решетки отдельных ионов. Действующие в ионных структурах силы обусловливают более прочную связь между частицами, чем межмолекулярные силы. Поэтому температура плавления и твердость веществ с ионной структурой значительно выше, чем веществ с молекулярной структурой. [51]
Особенно трудно провести границу между полярными и ионными молекулами. [52]
Казалось бы, что в чисто ионных молекулах мы встретимся с крайним случаем, когда центр тяжести электронного облака совпадает с центром аниона. [53]
Ионные пары в газовой фазе ( ионные молекулы) стабилизированы энергией Маделунга и дестабилизированы энергией Е %, затрачиваемой при образовании ионов. Наконец, связи А-В ссегда присуща ковалентная энергия, отвечающая перекрыванию орбиталей. [54]
Ослабление связи при присоединении иона к ионной молекуле или при объединении полярных молекул следует из электростатических соображений. [55]
К наиболее простым соединениям подобного типа относятся двухатомные ионные молекулы. Как и атом, молекула в целом электронейтральна. [56]
Во многих случаях МФК состоит в экстракции ионных молекул органическим растворителем или их растворении в нем. В связи с этим полезно иметь необходимые данные о структуре и свойствах таких растворов. Полный обзор этого предмета выходит за рамки настоящей книги. Однако в данном разделе будет представлено его краткое качественное изложение. [57]
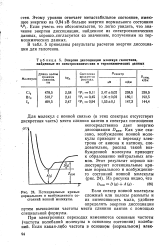 |
Энергии диссоциации молекул галогенов, найденные из спектроскопических и термохимических данных. [58] |
Хим - Как уже сказано, возбуждение ионной молекулы приводит к переходу электрона от аниона к катиону, следовательно, распад такой возбужденной молекулы приводит к образованию нейтральных атомов. [59]
Описанная ситуация во многом подобна ситуации для ионных молекул ( см., в частности, обсуждение LiF, приведенное в разд. Главное отличие состоит в том, что разность между потенциалом ионизации и сродством к электрону намного больше, чем в случае галогенидов щелочных металлов, так что при равновесном расстоянии ионное состояние может все еще иметь большую энергию, чем несвязывающее состояние. Второе отличие заключается в том, что для неионного состояния отсутствует ковалентное притяжение, так как оба электрона находятся на одной орбитади, так что потенциальная кривая для несвязывающей структуры будет отталкивательной или, самое большее, будет иметь неглубокий минимум. [60]
Страницы: 1 2 3 4 5