Моноалкилфенол
Cтраница 2
В последнее время развит метод анализа моноалкилфенолов по спектрам ЯМР в виде ацетильных производных [294], отличающийся тем преимуществом, что метильные радикалы ацетатных групп дают в три раза большую интенсивность сигнала по сравнению с сигналом протонов ОН-групп ( число протонов возросло с одного до трех) и занимают узкую область химических сдвигов при 2 1 ррт. Для орто-изрмера по сравнению с параизомером характерно поглощение в более слабом поле. [16]
 |
Метод алкилирования фенолов олефинами в присутствии катионитов. [17] |
Повышение температуры реакции также увеличивает выход моноалкилфенолов. [18]
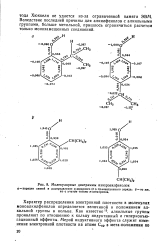 |
Молекулярные диаграммы изопропилфенолов. [19] |
Характер распределения электронной плотности в молекулах моноалкилфенолов определяется величиной и положением ал-кильной группы в кольце. Как известно15, алкильные группы проявляют по отношению к кольцу индуктивный и гиперконъю-гационный эффекты. [20]
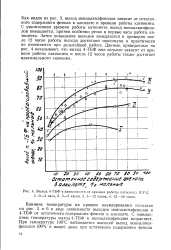 |
Выход 4 - ТБФ в зависимости от времени работы катионита КУ-2. 1. 0 - 3 часа. 2. 3 - 5 часов. 3. 5 - 12 часов. 4. 12 - 48 часов. [21] |
Как видно из рис. 3, выход моноалкилфенолов зависит от остаточного содержания фенола в алкилате и времени работы катионита. С увеличением времени работы катионита выход моноалкилфенолов повышается, причем особенно резко в первые часы работы катионита. Затем повышение выходов замедляется и примерно после 12 часов работы выхода достигают максимума и практически не изменяются при дальнейшей работе. Данные, приведенные на рис. 4-показывают, что выход 4 - ТБФ еще сильнее зависит от времени работы катионита и после 12 часов работы также достигает максимального значения. [22]
Рассмотренные выше катализаторы алкилирования позволяют получать смесь изомерных моноалкилфенолов, из которых преобладающим является л-изомер. Преимущественное образование о-изомера возможно только в определенных условиях. Поэтому до недавнего времени о-алкилфенолы, свободные от п-изомеров, в промышленном масштабе не получали. Известные ранее способы получения орто-соединений [77 - 79] исходили из галоген-производных и не были экономически целесообразными. [23]
С бифункциональными фенолами ( например, с моноалкилфенолами) формальдегид может образовывать только линейные термопластичные смолы. Образуются ли при взаимодействии формальдегида с трехфункциональными фенолами термопластичные или термореактивные смолы, зависит от количества альдегида или фенола ( избыток или недостаток) и от характера катализатора. [24]
С бифункциональными фенолами ( например, с моноалкилфенолами) формальдегид может образовывать только линейные термопластичные полимеры. Образуются ли при взаимодействии формальдегида с трехфункциональными фенолами термопластичные или термореактивные полимеры, зависит от количества альдегида или фенола ( избыток или недостаток) и от характера катализатора. [25]
С бифункциональными фенолами ( например, с моноалкилфенолами) формальдегид может образовывать только линейные термопластичные смолы. Образуются ли при взаимодействии формальдегида с трехфункциональными фенолами термопластичные или термореактивные смолы, зависит от количества альдегида или фенола ( избыток или недостаток) и от характера катализатора. [26]
Таким образом, если сопоставить наиболее эффективный бис-фенол с наиболее эффективным моноалкилфенолом, то при использовании их в смесях с фосфонатом противоокислительная активность первого в 10 раз превышает активность второго. [27]
Благодаря этому повышается выход и степень чистоты232 наиболее ценных для практики моноалкилфенолов. Так, в алкилате, полученном в присутствии ионитов, содержится в 5 - 6 раз меньше примесей, чем при использовании других катализаторов232, в отдельных же случаях образуются преимущественно244 или только245 моноалкилфенолы. [28]
Поэтому при повышении активности катализатора, температуры и продолжительности реакции содержание моноалкилфенола в получаемой смеси может значительно возрасти. [29]
 |
Схема синтеза алкилсалицилатов. [30] |
Страницы: 1 2 3 4