Монокетон
Cтраница 1
Монокетоны относятся к наименее кислым соединениям, анионы которых стабилизованы за счет резонанса. Они являются несколько более сильными кислотами, чем соответствующие суль-фоны, цианиды и сложные эфиры карбоновых кислот, но значительно слабее аналогичных нитроалканов, р-кетоэфиров и малоновых эфиров. [1]
Монокетоны и нитрилы можно алкилировать так же, как и р-дикарбонильные соединения. В силу их меньшей кислотности в этом случае приходится использовать грег-бутилат калия или амид натрия. [2]
Монокетоны относятся к наименее кислым соединениям, анионы которых стабилизованы за счет резонанса. Они являются несколько более сильными кислотами, чем соответствующие суль-фоны, цианиды и сложные эфиры карбоновых кислот, но значительно слабее аналогичных нитроалканов, р-кетоэфиров и малоновых эфиров. [3]
Монокетоны, имеющие ароматическое ядро в соседстве с карбонильной группой, образуют оксикетон и ароматическую кислоту, но дают лишь следы перекиси или вовсе ее не дают. [4]
Монокетоны были получены при нагревании хлорангидридов кислот с несколькими частями ароматических углеводородов, если нужно в присутствии сероуглерода в качестве растворителя, и с последующей обработкой небольшими порциями, несколько большим количеством, чем вычислено, хлористого алюминия. [5]
Алифатические монокетоны образуют всегда перекись и а-оксикетон. [6]
Ненасыщенные монокетоны IV и V, по-видимому, не имеют заметного эффективного дипольного момента, поскольку амплитуды кругового дихроизма этих соединений почти одни и те же в каждом из растворителей. Это не удивительно, так как дипольный момент карбонильной группы направлен вдоль оси хромофора и вследствие симметрии влияния матрицы, образованной молекулами растворителя, сводится к нулю. В круговом дихроизме заметное влияние могут оказать только структурные изменения в непосредственной близости от хромофора. Поэтому дипольные моменты гидроксильных групп не играют существенной роли. Ненасыщенные кетоны VI и VII также имеют малый эффективный дипольный момент. Иные результаты были получены для соединения VIII, однако в настоящее время для них нет объяснения. [7]
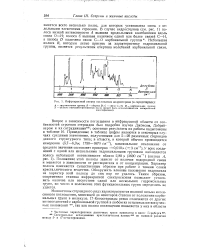 |
Инфракрасный спектр поглощения андростерона ( в сероуглероде. [8] |
Монокетоны стероидного ряда характеризуются полосой весьма интенсивного поглощения, зависящей до некоторой степени от положения карбонильных групп в молекуле. [9]
Гидразоны насыщенных монокетонов и альдегидов е этих условиях не разлагаются. Так, гидразон энантового альдегида не изменяется при кипячении в течение 50 час. [10]
Кривая КД монокетона ( IX) характеризуется исключительно большой интенсивностью. [11]
Так же как для монокетонов, для р-дикетонов наблюдается процесс распада по у-связи в концевой н-алкильной цепи, непосредственно присоединенной к карбонильной группе, или в алкиль-ном заместителе. [12]
MgJ, при котором образуется монокетон, и радикального СНз MgJ, приводящего к образованию дикетона, необходимо учитывать, что ионный механизм в данном случае затруднен в связи с пространственными препятствиями у исходного хлорангидрида, избыток которого может быть восстановлен MgJ. Тем самым появляется возможность течения реакции по радикальному механизму. [13]
Оказалось, что димедон подобно монокетонам легко реагирует с тиомочевиной в присутствии галогена. Наилучшие выходы аминатиазола ( I) получены при взаимодействии димедона с тиомочевиной в присутствии йода. [14]
Оказалось, что димедон подобно монокетонам легко реагирует с тиомочевиной в присутствии галогена. Наилучшие выходы аминотиазола ( I) получены при взаимодействии димедона с тиомочевиной в присутствии йода. [15]
Страницы: 1 2 3 4