Моноксид - азот
Cтраница 2
Ели-нек впервые экспериментально определил скорость разложения моноксида азота в интервале температур 690 - 1750 С при атмосферном давлении и на основании найденной закономерности рассчитал скорость этой реакции для более высоких и низких температур. [16]
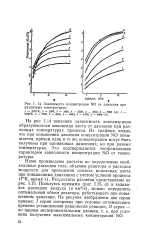 |
Зависимость концентрации NO от давления при различных температурах. [17] |
На рис. 1.14 показана зависимость концентрации образующегося моноксида азота от давления при различных температурах процесса. Из графика видно, что при повышении давления концентрация NO повышается, причем одни и те же концентрации могут быть получены при одинаковых давлениях, но при разных температурах. Это подтверждается экстремальным характером зависимости концентрации NO от температуры. [18]
Уменьшение объема обусловлено присоединением кислорода к моноксиду азота. Из уравнения реакции моноксида азота с кислородом видно, что 2 объема моноксида азота реагируют с 1 объемом кислорода, образуя 2 объема диоксида азота. При этом объем смеси уменьшается на единицу. Поскольку по условию задачи объем уменьшается на 100 мл, то это значит, что 100 мл кислорода прореагировали с 200 мл моноксида азота с образованием 200 мл диоксида азота. [19]
Пропуская воздух через электрическую дугу, получают моноксид азота. [20]
В табл. 1.3 приведена зависимость времени релаксации моноксида азота от температуры для воздуха при атмосферном давлении. [21]
По условию задачи смешивают 40 мл смеси моноксида азота с 65 мл воздуха, с держащего 13 мл кислорода и 52 мл азота. [22]
 |
Структура Р, ( а, Р406 ( б и Р4О 0 ( в. [23] |
Азотистая кислота неустойчива и диспропорциони-рует на азотную кислоту и моноксид азота ( разд. Структура ее может быть представлена в виде ( б) с делокализованной л-связью. [24]
При смешивании 60 мл моноксида углерода, 40 мл моноксида азота и 120 мл воздуха, содержащего 24 мл кислорода ( 20 %) и 96 мл азота ( 80 %), диоксид азота прореагирует с кислородом. По уравнению реакции моноксида азота с кислородом 2 мл моноксида азота прореагируют с 1 мл кислорода, образуя 2 мл диоксида азота, а 40 мл моноксида азота прореагируют с 20 мл кислорода, образуя 40 мл диоксида азота. Моноксид углерода и азот при этом остаются без изменений. Образовавшаяся смесь состоит из 60 мл моноксида углерода, 40 мл диоксида азота, 96 мл азота и 4 мл ( 24 - 20 4) кислорода. [25]
Ранее было установлено, что кривая, характеризующая зависимость концентрации моноксида азота от температуры, имеет перегиб при Г3500 - 3600 К, когда максимальные концентрации моноксида азота достигают - 5 % для воздуха при давлении 1 ата. [26]
Основанием для такого выбора является направление валентностей в молекулах кислорода и моноксида азота. [27]
На третьей гранке номограммы показано влияние состава азотно-кислородной смеси на концентрацию моноксида азота при обогащении воздуха кислородом. [28]
Основанием для такого выбора является направление валентностей в молекулах кислорода и моноксида азота. [29]
Следовательно, добавка метана к азотно-кислород-ным смесям во всех случаях снижает выход моноксида азота в состоянии равновесия. [30]
Страницы: 1 2 3 4