Моноксид - азот
Cтраница 4
Установки, работающие на твердом и жидком топливе, а также на газе, с термическим режимом свыше 400 МВт должны быть оснащены измерительными приборами для непрерывного определения массовой концентрации моноксида азота и диоксида азота в отработанном газе. Если измерения показывают, что доля диоксида азота в эмиссиях моноксида азота не превышает 5 %, непрерывный мониторинг может быть прекращен, а доля диоксида азота определяется расчетным путем. При необходимости непрерывных измерений диоксида азота установка должна быть оснащена соответствующим измерительным оборудованием в шестимесячный срок со дня пуска. [46]
Этому способствует ионизация компонентов значительного повышения среднемассовой темпе-реакции с образованием ионов азота и кисло-которые быстро реагируют с молекулярным азо - - том или кислородом с малой или нулевой энергией ак - гивации и образуют моноксид азота. [47]
Содержание моноксида азота в конечном газе в значительной мере зависит от скорости охлаждения системы NO - N2 - О2 - О - N до температур ниже 2000 К, при которых скорость термического разложения моноксида азота незначительна. В процессе медленного охлаждения системы большая часть моноксида азота разлагается. При быстром охлаждении имеет место эффект закалки моноксида азота, в результате чего система приходит к термодинамически неравновесному состоянию. [48]
В монографии приведены общие сведения о низкотемпературной плазме и методах ее получения, рассмотрены физико-химические основы окисления азота в плазме, показано влияние технологических параметров на процесс окисления азота воздуха, описана опытно-промышленная установка для синтеза моноксида азота. [49]
Можно ли сделать вывод, что а) реакция является тримолекулярной, б) реакция протекает в одну стадию, в) реакция имеет в целом третий порядок, г) реакция имеет первый порядок как по кислороду, так и по моноксиду азота. [50]
Из данных этих таблиц видно, что при увеличении количества воды в исходной смеси концентрации NO в охлажденном газе резко возрастает и достигает 11 48 % для смеси H2O: NO4 и 13 85 % - для смеси Н2О: ( 0 2О2 0 8N2) 4, причем максимальные значения концентраций моноксида азота сдвигаются в сторону более высоких температур. [51]
Скорость образования моноксида азота в зависимости от температуры при атмосферном давлении впервые была определена К. [52]
При смешивании 60 мл моноксида углерода, 40 мл моноксида азота и 120 мл воздуха, содержащего 24 мл кислорода ( 20 %) и 96 мл азота ( 80 %), диоксид азота прореагирует с кислородом. По уравнению реакции моноксида азота с кислородом 2 мл моноксида азота прореагируют с 1 мл кислорода, образуя 2 мл диоксида азота, а 40 мл моноксида азота прореагируют с 20 мл кислорода, образуя 40 мл диоксида азота. Моноксид углерода и азот при этом остаются без изменений. Образовавшаяся смесь состоит из 60 мл моноксида углерода, 40 мл диоксида азота, 96 мл азота и 4 мл ( 24 - 20 4) кислорода. [53]
Уменьшение объема обусловлено присоединением кислорода к моноксиду азота. Из уравнения реакции моноксида азота с кислородом видно, что 2 объема моноксида азота реагируют с 1 объемом кислорода, образуя 2 объема диоксида азота. При этом объем смеси уменьшается на единицу. Поскольку по условию задачи объем уменьшается на 100 мл, то это значит, что 100 мл кислорода прореагировали с 200 мл моноксида азота с образованием 200 мл диоксида азота. [54]
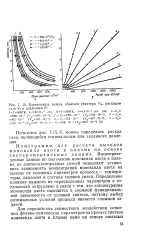 |
Взаимосвязь между объемом реактора Vf, расходом газа Уг и давлением Р. [55] |
Вышеприведенные данные по получению моноксида азота в плазме из азотно-кислородных смесей позволяют установить зависимость концентраций моноксида азота на выходе от основных параметров процесса - температуры, давления и состава газовой смеси. Определение влияния каждого из перечисленных параметров в отдельности затруднено в связи с тем, что концентрация моноксида азота находится в сложной функциональной зависимости от условий синтеза, поэтому выбор оптимальных условий процесса является сложной задачей. [56]
Происходит это оттого, что образовавшийся моноксид азота, присоединяя кислород, снова переходит в диоксид азота. [57]
Интерес представляет также влияние небольших добавок моноксида азота к плазме на процесс синтеза NO. При подогреве воздуха до температур 2000 - 2500 К в процессе горения, а также при использовании некоторых методов выделения оксидов азота из газовой смеси, в послед - ней остается некоторое количество NO, поэтому целесообразно эту газовую смесь направлять в плазмотрон, что позволяет избежать выбросов NO в атмосферу. [58]
Содержание моноксида азота в конечном газе в значительной мере зависит от скорости охлаждения системы NO - N2 - О2 - О - N до температур ниже 2000 К, при которых скорость термического разложения моноксида азота незначительна. В процессе медленного охлаждения системы большая часть моноксида азота разлагается. При быстром охлаждении имеет место эффект закалки моноксида азота, в результате чего система приходит к термодинамически неравновесному состоянию. [59]
Страницы: 1 2 3 4