Моноксид - азот
Cтраница 3
Интересная проблема возникает при попытке записать льюисову структурную формулу молекулы распространенного загрязнителя воздуха моноксида азота, NO. Для этой молекулы не удается построить конфигурацию с замкнутыми оболочками, потому что в ней нечетное число валентных электронов. Действительно, в NO 11 валентных электронов, пять из которых первоначально принадлежали атому азота, а шесть-атому кислорода. Таким образом, в молекуле NO атом азота или атом кислорода будет окружен только семью, а не восемью электронами. Поскольку азот-менее электроотрицательный элемент, чем кислород, следует ожидать, что неполное окружение должно быть именно у этого атома. [31]
 |
Радиальный конвертер мо-ноксида углерода. [32] |
Реакторы с катализатором в виде нескольких слоев платиновой сетки применяют для окисления аммиака в моноксид азота. Такой реактор ( контактный аппарат), работающий под давлением 0 8 МПа при температуре 850 - 900 С, показан на рис. 4.44. Корпус аппарата состоит из двух полых усеченных конусов / и 3, снабженных фланцами и соединенных большими основаниями. [33]
 |
Контактный аппарат для окисления аммиака. [34] |
Реакторы с катализатором в виде нескольких слоев платиновой сетки применяют для окисления аммиака в моноксид азота. Такой реактор ( контактный аппарат), работающий под давлением 0 8 МПа при температуре 850 - 900 С, показан на рис. 5.43. Корпус аппарата состоит из двух полых усеченных конусов / и 3, снабженных фланцами и соединенных большими основаниями. [35]
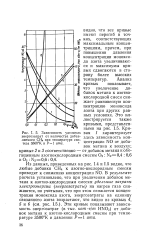 |
Зависимость удельных энергозатрат от количества добав-ляемого СН4 при температуре син-теза 3500 К и Р1 ата,. [36] |
Анализ кривых показывает, что увеличение добавок метана к азотно-кислородной смеси снижает равновесную концентрацию моноксида азота при других равных условиях. [37]
С целью определения энергозатрат на единицу получаемого продукта на IV гранке нанесена зависимость энергозатрат от условий процесса и концентраций получаемого моноксида азота. [38]
Зависимость концентрации моноксида азота от содержания в смеси кислорода построена в координатах Хр и XNQ, где XNO - концентрация моноксида азота с учетом температуры, давления и состава смеси при синтезе NO из азотно-кислородной смеси. [39]
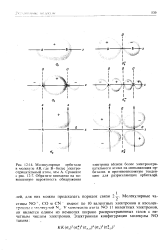 |
Молекулярные орбитали в молекуле АВ, где В - более электроотрицательный атом, чем А. Сравните с 12 - 7. Обратите внимание на повышенную вероятность обнаружения. [40] |
Молекулярные частицы NO, СО я CN - имеют по 10 валентных электронов и изоэлек-тронны с молекулой N2, У моноксида азота NO 11 валентных электронов, он является одним из немногих широко распространенных газов с нечетным числом электронов. [41]
В расчете приняты следующие обозначения: ПА и п-в - соответственно количество килограмм-молекул азота и кислорода в исходной смеси и X-количество килограмм-молекул моноксида азота в равновесной смеси. [42]
Ранее было установлено, что кривая, характеризующая зависимость концентрации моноксида азота от температуры, имеет перегиб при Г3500 - 3600 К, когда максимальные концентрации моноксида азота достигают - 5 % для воздуха при давлении 1 ата. [43]
Как только бесцветный газ, выходящий из газоотводной трубки, при соприкосновении с воздухом начнет буреть, конец газоотводной трубки подвести под цилиндр и наполнить его моноксидом азота. [44]
В экспериментальных исследованиях, в качестве плазмообразующих газов были испытаны воздух, аргон, чистый азот, аргоно-азотная смесь, воздух с добавками воды, метана, диоксида углерода, моноксида азота. [45]
Страницы: 1 2 3 4