Моносахарид
Cтраница 1
Производные моносахаридов, содержащие вместо первичной спиртовой группы карбоксильную; получаются гидролизом природных соединений или окислением первичной спиртовой группы моносахаридов. [1]
Ацетонпроизьодные моносахаридов, которые называются также изопропил-иденпроизводными, образуются преимущественно таким образом, что каждая изопропилиденсвая группа замещает атомы водорода двух соседних гидрокси-лов, находящихся в цие-положении. [2]
Ацетонпроизьодные моносахаридов, которые называются также изопропил-иденпроизводными, образуются преимущественно таким образом, что каждая изопропилиденсвая группа замещает атомы водорода двух соседних гидрокси-лов, находящихся в цис-положенни. [3]
Производные моносахаридов в кольчатой форме, в которых атом водорода полуацетального гидроксила замещен каким-либо радикалом, называют глюкозидами. Соединение, вступившее во взаимодействие с полуацетальным гидро-ксилом, называют аглюконом. [4]
Кетопроизводные моносахаридов ( альдозулозы) получают окислением вторичных гидроксигрупп свободных сахаро. Однако этот метод дает хорошие результаты в случае соответствующим образом ьчащищен-ных производных. В этом случае редко удается выделить свободную альдозулозу, однако такие производные широко используют в качестве полупродуктов. Еще одной сложностью является то, что свободные альдозулозы обычно не кристаллизуются из-за большого числа циклических форм, в которых они могут существовать. [5]
Производные моносахаридов активно участвуют в метаболизме живой клетки. С их многообразными превращениями связаны фотосинтез, обеспечение клетки энергией, детоксикация и вывод ядовитых веществ, проникающих извне или возникающих в ходе метаболизма, биосинтез ароматических аминокислот - тирозина и фенилаланина, а также ряда других ароматических соединений, образование сложных биополимеров ( полисахаридов, гликопротеинов, гликолипидов, нуклеиновых кислот), которые играют главную роль в построении субклеточных структур, обеспечивающих правильное функционирование клетки. [6]
Производные моносахаридов по полуацетальному гидроксилу следует рассматривать как продукты замещения этого гидроксила на анионоидные группы, что соответствует реальным путям образования большинства этих соединений. [7]
Оксазолиновые производные моносахаридов, поскольку они устойчивы в щелочной, нейтральной и слабокислой средах, были использованы для синтеза 2 6-диаминосахаров, обнаруженных в последнее время в различных антибиотиках. В таких синтезах оксазолиновый цикл выполняет функцию защитной группировки, блокирующей амино - и оксигруппу одновременно. После введения в молекулу моносахарида второй аминогруппы оксазолиновая защита снимается кислотным гидролизом. [8]
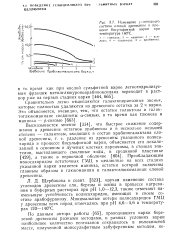 |
Изменение углеводного состава еловой древесины в процессе бисульфитной варки при температуре 160 С. / - глюкоза. 2 - манноза. 3 - ксилоза. 4 - галактоза. 5 - арабнноза. [9] |
Преобладающим моносахаридом остаточных ГМЦ в целлюлозе на всех стадиях указанной варки является манноза, остатки которой включены главным образом в глюкоманнан и галактоглюкоманнан еловой древесины. [10]
Главным моносахаридом, входящим в состав выделенных таким образом пектиновых веществ, является D-галактуроновая кислота, в малых количествах обычно присутствуют L-арабиноза и D-галактоза, реже - L-рамноза, D-ксилоза, L-фукоза и др. Часть остатков уроновых кислот в пектиновых веществах этерифицирована метиловым спиртом. Такие частично этерифицированные полиурониды обычно называют пектиновыми кислотами, а родоначальные поликарбоксильные соединения - пектовыми кислотами. [11]
Единственным моносахаридом, входящим в состав крахмала, является D-глюкоза. Тем не менее крахмал представляет собой смесь полисахаридов. Весьма своеобразным свойством амилозы является способность этого полисахарида образовывать комплексы с многочисленными полярными органическими молекулами. Осаждение комплекса амилозы, чаще всего с н-бутанолом 169, позволяет получить ее в высокоочищенном состоянии; амилопектин, выделяемый из маточных растворов, обычно бывает загрязнен некоторым количеством амилозы. [12]
Синтез моносахаридов из моносахаридных же предшественников удобен, разумеется, тем, что большая часть целевой структуры уже имеется в исходном соединении: весь углеродный скелет или, по крайней мере, его значительная часть, большинство функциональных групп, нужная конфигурация большинства асимметрических центров. Однако именно в этом и заключается главная трудность. Ведь для того, чтобы выполнить целенаправленную трансформацию, нужно суметь не затронуть другие, химически весьма близкие группировки в исходной молекуле. Например, при синтезе 4 - 0-метил - В-глюкуроновой кислоты ( 3) нужно тем или иным способом обеспечить мети лирование именно четвертого гидроксила, а не весьма сходных с ним по химическим свойствам третьего или второго. Аналогично для превращения D-ксилозы ( 11) в D-ликсозу ( 10) надо добиться обращения конфигурации углеродного атома С-2, несущего в пиранозной форме экваториальный вторичный гидроксил, и не затронуть при этом конфигурацию двух других центров ( G-3 и С-4), также находящихся в пиранозном цикле и также связанных с экваториальными вторичными гидроксилами. Аналогичные задачи возникают в каждом из приведенных выше принципиальных синтетических путей и практически в каждом другом синтезе моносахаридов по схеме трансформаций. [13]
Восстановление моносахаридов может осуществляться не только при действии восстановителей ( газообразный водород, амальгама натрия и др.), но также в организме ферментативным путем. Образующиеся спирты имеют важное биологическое значение. Так, спирт рибитол входит в состав витамина В2 ( рибофлавин) и ряда коферментов. [14]
Номенклатура моносахаридов основывается на соединениях с не разветвленной цепью атомов углерода. Углеродные атомы нумеруют таким образом, чтобы карбонильный углерод имел наименьший номер. Заместители ( атомы, функциональные группы) получают тот же номер, что и углеродный атом, с которым они соединены. Если в молекуле имеется более одной функциональной группы, они перечисляются в алфавитном порядке. [15]
Страницы: 1 2 3 4