Нарушение - копланарность
Cтраница 1
 |
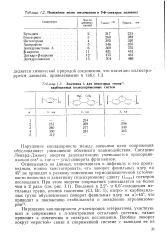
Положение полос поглощения в УФ-спектрах полиенов.| Значения А для некоторых типов31 карбоцепных полисопряженных систем. [1] |
Нарушение копланарности между звеньями цепи сопряжения обусловливает уменьшение обменного взаимодействия. Согласно Ленард-Джонсу энергия делокализации уменьшается пропорционально cos2 а, где а - угол поворота фрагментов. [2]
Нарушение копланарности в результате выведения нитрогруппы из плоскости бензольного кольца должно затруднить энергетически выгодное я-сопряжение в р-нитростиролах и в а-фурил-р-нитро - этилене и приблизить их моменты к моментам алифатических нитросоединений, что не имеет места. Следовательно, предположение о некопланарности исследованных веществ также отпадает. [3]
Нарушение копланарности не Связано только с поворотом вокруг единичной связи С-С в бутадиеновой системе, так как в этом случае коэффициенты интенсивности в исследованных ( Va и V6) и модельном соединениях ( IV) были бы одинаковы. [4]
Нарушение копланарности аминов ослабляет сопряжение аминогруппы с ядром и повышает основность аминов. [5]
 |
Положение полос поглощения в УФ-спектрах полиенов.| Значения А для некоторых типов31 карбоцепных полисопряженных систем. [6] |
Нарушение копланарности р-электронов гетероатома, участвующих в сопряжении с я-электронами остальной системы, также приводит к изменению в спектрах поглощения. [7]
Результатом нарушения копланарности является ослабление я-сопряжения в р-метил-р-нитростиролах с участием бензольного кольца, винильнои и нитрогрупп; однако сохраняется менее эффективное я, а-сопряжение С - Н - связей метильной группы и двойных связей винильного остатка. [8]
Происходящее при этом нарушение копланарности уменьшает сопряжение карбонильной группы с бензольным ядром, благодаря чему увеличивается нуклеофильность атомов углерода ядра, в том числе и атома углерода, связанного с ацильным остатком. В резуль тате этого орго-замещенные кетоны дезацилируются значительно легче, чем изомеры, лишенные стерических препятствий нормальному разме щению ацильной группы. [9]
Наиболее частой причиной нарушения копланарности являются особенности геометрии молекулы, например наличие объемистых заместителей, не позволяющих взаимодействующим группам принять плоскую конформацию. Ниже будут рассматриваться именно такие случаи, относящиеся к полярному сопряжению. [10]
Выяснено, что при нарушении копланарности ауксохрома и ароматического ядра полоса поглощения перемещается в коротковолновую часть спектра. [11]
 |
Пространственные препятствия в молекуле N. N-диметил-о - толу-идина. [12] |
Выяснено, что при нарушении копланарности ауксохрома и ароматического ядра полоса поглощения перемещается в коротковолновую часть спектра. [13]
Однако пространственные препятствия, вызывающие нарушение копланарности и выключение действия нитрогруппы, могут существенно изменить эту картину. [14]
Как при сохранении, так и при нарушении копланарности металлоорганической группировки с ароматическим кольцом экранирование фтора возрастает в результате координации. Это обусловлено большей чувствительностью химического сдвига фтора к увеличению электронной плотности на сопряженном с кольцом заместителе в тг-положении, чем к ее эквивалентному уменьшению на заместителе в - положении. Необходимо отметить, что рост ХСЗ металлоорганических группировок при переходе от фторфенолятов к бромзамещенным аналогам можно было бы, по крайней мере в принципе, объяснить увеличением электроноакцептор-ной способности феноксильной группы при введении атомов брома. Сравнение относительного роста ХСЗ для группировок ( C6H6) 3SnO - и C6H5HgO - при переходе от 2-фторфенолятов к 2 6-дибромзамещенным показывает, что в последнем случае имеет место более сильная координация металлоорганической группировки с атомом галогена. Аналогичное рассуждение приводит к выводу, что образование внутримолекулярной водородной связи с атомом брома сопровождается меньшим переносом электронной плотности, чем в случае координации ртутноорганической группировки с атомом галогена. [15]
Страницы: 1 2 3 4