Белок
Cтраница 3
Белок является полифункциональным соединением, в котором каждый аминокислотный остаток выполняет определенную роль в поддержании нативиой конформации или проявлении биологической функции. Если используются модифицирующие агенты достаточно широкой специфичности, конечный результат зависит от доступности тех или иных функциональных групп белка в данных условиях. Этот прием широко применяется и для исследования топографии мембранных белков, когда доступными действию так называемых непроникающих реагентов оказываются лишь группировки, расположенные вне мембраны. [31]
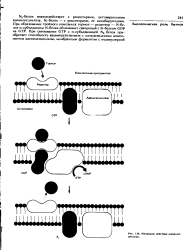 |
Механизм действия адснилат. [32] |
Белок взаимодействует с рецепторами, активирующими аденилатциклазу, Ni-белок - с рецепторами, ее ингибирующими. [33]
Белки - макромолекулярные природные вещества ( биополимеры), структурную основу которых составляют полипептидные цепи, построенные из а-аминокислотных остатков. [34]
Белки - высокомолекулярные полипептиды, представляют собой сложные биополимеры. Их различают по составу и форме молекул. [35]
Белки обладают большой молекулярной массой. [36]
Белки в природе синтезируются из аминокислот. При гидролизе белков сначала образуются растворимые в воде промежуточные продукты - альбумозы и пептоны, которые затем распадаются на аминокислоты. [37]
Белки, как и полисахариды, представляют собой ангидриды, которые при гидролизе присоединяют воду и распадаются на простейшие вещества - гидраты или аминокислоты. Гидролиз белков протекает в нескольких фазах: вначале образуются альбумозы и пептоны, а затем аминокислоты. Таким образом, для эффективного осуществления процессов гидролиза крахмала и белков в заторном аппарате требуется создать оптимальные условия концентрации и температуры среды. [38]
Белки очень легко усваиваются бактериями. В анаэробной обстановке, возникакЛцей в донных илах, могут сохраняться продукты неполного разложения белков и соединения их с другим: и веществами. В частности, при конденсации аминокислот с углеводами образуются вещества, которые впоследствии преобразуются в гуминовые кислоты, по химическому составу и строению отличающиеся от гуминовых кислот торфов и углей. [39]
Белки гидролизуются в пептиды и далее в аминокислоты, поступающие в клетку, где они дезаминируются и превращаются в органические кислоты. Однако часть аминокислот, например аргинин, разлагается своими путями. У анаэробных протеолитичес-ких организмов имеются различные пути брожения аминокислот и других органический соединений азота. Конечными продуктами здесь являются аммиак, жирные кислоты, обычно разветвленные, и ацетат. [40]
 |
Влияние разрушения S-S - связей на прочность межфазного адсорбционного слоя - казеина на границе водный раствор - казеина / углеводород при рН 10 8 и 20 С. [41] |
Белки очень чувствительны к изменению активности водородных ионов в связи с множеством способных к ионизации групп в молекуле. Для выяснения роли заряда молекул глобулярных белков на скорость образования адсорбционного слоя и величину прочности, а также на время жизни элементарных капель нами изучалось поведение межфазных слоев глобулярных белков при разных рН среды от 2 до 10 и 22 и 55 С. [42]
Белки, содержащиеся в муке, при быстром высушивании ( 130 - 135 С, 1 ч) денатурируются в меньшей степени, чем после нагревания в течение 6 ч при 105 С. [43]
Белки являются полимерами, в которых фрагменты а-аминокислот соединены амидными связями. Для построения белков природа использует 20 а-аминокислот. [44]
Белки - это полиамиды, образованные самыми разнообразными сочетаниями природных ос-аминокислот. Для нормальной работы белка в биологической системе исключительно важна последовательность аминокислот в полипептидной цепи. Эта последовательность может быть определена при применении различных методов. [45]
Страницы: 1 2 3 4