Белок - плазма
Cтраница 3
Достаточно полно изучен качественный и количественный состав белков плазмы крыс, подвергнутых пролонгированному облучению. До 12 - х суток после облучения в дозе 116 1 мКл / кг рентгеновскими лучами с мощностью дозы 8 6 - 10 - 6 А / кг количество альбуминов и суммарного белка сохраняется на пониженном уровне. При ежесуточном облучении в дозе 25 8 мКл / кг за сутки содержание преальбумина и трансферрина не изменяется до 39 - х суток ( суммарная доза 1006 мКл / кг), тогда как содержание Ai-макроглобулина и 3-го компонента комплемента повышается. К моменту гибели животных ( 39 - 40 - е сутки облучения) концентрация всех этих белков уменьшается. [31]
Применение методов математического моделирования при изучении процессов обмена белков плазмы представляет собой одну из важнейших особенностей исследования указанных процессов. Оценка кинетических характеристик процесса обмена производится в соответствии с заранее выбранной моделью процесса, являющейся формальным выражением связей в изучаемом процессе. Второй особенностью исследований обмена белков плазмы является то, что эти исследования проводятся на основе наблюдений за поведением белка, меченного изотопами 7 или J Несмотря на разнообразие моделей процесса обмена белков, при их построении используется общая идея условного разделения организма на ряд отделов, между которыми наблюдается транспорт метаболитов. Специфические особенности экспериментов с иодированными белками определяют ограниченность информации, на основе которой производится оценка кинетических характеристик процесса. Естественно, что точность полученных оценок существенно зависит от того, насколько точно модель процесса отображает сам процесс. [32]
Метод электрофореза широко применяют в клинике для анализа белков плазмы и сыворотки крови. Сыворотка крови представляет собой плазму, лишенную фибриногена. При заболеваниях может изменяться как общее количество белков плазмы, так и содержание отдельных белков или белковых фракций без изменения общего количества белка. Напротив, острые инфекционные заболевания, возникновение некоторых злокачественных новообразований сопровождаются повышенным содержанием белков в крови, чаще всего глобулиыовой фракции. Поэтому анализ белков сыворотки крови имеет большое диагностическое значение и позволяет наблюдать за ходом лечения. Суммарный заряд белковой молекулы изменяется в зависимости от рН и при определенном значении рН ( изоэлектриче-ская точка) равен нулю. Белок в изоэлектрическом состоянии при электрофорезе не передвигается ни к катоду, ни к аноду, наименее устойчив в растворе и при стоянии выпадает в осадок. [33]
Валасек и Хаггинс [2411] обнаружили, что при обработке белков плазмы сырыми препаратами а-амилазы образуется пептид, обладающий гипертензивной активностью; этот пептид был назван веществом А. Позднее было показано [1077, 2411, 2412], что вещество А не образуется в присутствии ингибиторов а-амилазы. В то же время кристаллические препараты ос-амилазы, выделенные из различных источников, не всегда приводят к образованию вещества А. Эти результаты позволили предложить двухстадийный механизм процесса образования вещества А, в котором принимают участие не тодько ос-амилаза, но и протео-литические ферменты, присутствующие в качестве примесей в сырых препаратах амилазы. [34]
Это действие глицина и органических растворителей используется при фракционировании белков плазмы ( см. гл. При повышении диэлектрической постоянной усиливается ионизация белков, чем и объясняется повышение их растворимости. [35]
Примером этих белков могут служить яичный альбумин, казеин и белки плазмы. Гисто-ны и протамины отличаются от других глобулярных белков высоким содержанием основных аминокислот, что видно из данных, приведенных в табл. 42 ( стр. Протамяны найдены только в зрелой сперме разных видов рыб. [36]
Уже в стадии подозрения на силикоз нарушена проницаемость капилляров для белков плазмы; процент случаев изменения проницаемости нарастает с усилением силикотического процесса. [37]
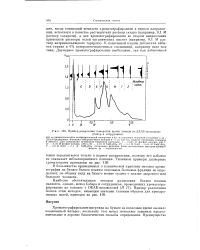 |
Пример разделения сыворотки крови лошади на ДЕАЕ-цсллюлозе. [38] |
В большинстве применяемых в клинической практике методов хроматографии на бумаге белков плазмы отдельные белковые фракции не определяют; по общему виду на бумаге можно судить о плазме здорового или больного человека. [39]
В клинической практике встречаются состояния, характеризующиеся изменением общего количества белков плазмы: гипопротеинемия, диспротеине-мия, гиперпротеинемия. [40]
В последние годы появляются сообщения о механизмах выхода из сосудов белков плазмы путем включения их в состав оезикул и дальнейшего транспортирования этих белков через цитоплазму эидотелиальных клеток. [41]
Важнейшими буферами крови являются бикарбонаты и фосфаты Na и К, белки плазмы и особенно гемоглобин эритроцитов. Механизм действия бикарбонатов и фосфатов как буферов, препятствующих изменению рН крови при появлении в ней кислот или оснований, подробно рассмотрен в главе Водно-солевой обмен ( стр. [42]
Важнейшими буферами крови являются бикарбонаты и фосфаты Na и К, белки плазмы иособенно гемоглобин эритроцитов. Механизм действия бикарбонатов и - фосфатов как буферов, препятствующих изменению рН крови при появлении в ней кислот или оснований, подробно рассмотрен в главе Водно-солевой обмен ( стр. [43]
Так как реакция крови сдвинута в щелочную сторону от изоэлект-рических точек белков плазмы и гемоглобина, то эти белки находятся в крови в виде поливалентных анионов. [44]
Накоплены данные о предпочтительном связывании тех или иных металлов с отдельными фракциями белков плазмы или форменными элементами. В ряде случаев эти сведения еще противоречивы. По одним данным, цинк накапливается в эритроцитах, а еще больше - в лейкоцитах; по другим - основное количество этого металла сосредоточено в безбелковом фильтрате крови, небольшое - связано с гамма-глобулинами, а около 25 % - с альбуминами. По Vallee ( 1956, 1959), транспорт цинка скорее осуществляется в виде слабо связанного белкового комплекса. [45]
Страницы: 1 2 3 4