Мышечные белок
Cтраница 1
Мышечные белки представляют большой интерес в особенности по той причине, что они обладают свойствами, обусловливающими способность, мышц к сокращению. [1]
Мышечные белки могут быть разделены на ряд фракций, более или менее резко отличающихся друг от друга по растворимости в воде и солевых растворах с различной ионной силой. [2]
Мышечные белки представляют большой интерес в особенности потому, что они обладают свойствами, обусловливающими способность мышц к сокращению. [3]
Мышечные белки могут быть разделены на ряд фракций, более или менее резко отличающихся друг от друга по растворимости в воде и солевых растворах с различной ионной силой. [4]
Остальные мышечные белки находятся в незначительных количествах. Приведенное распределение основных фракций мышечных белков не является постоянным и значительно меняется в процессах посмертных изменений мышечной ткани, сопровождающихся переходом части растворимых белков в нерастворимое состояние. В живой мышце миоген и глобулин X входят в состав саркоплазмы, а миозин и актин - в состав мио-фибриллей. [5]
Периодическое изменение физического состояния мышечных белков, обусловливающее возможность попеременного сокращения и расслабления мышц и выполнения механической работы, очевидно, каким-то образом, связано с важнейшими, дающими энергию обменными химическими процессами. [6]
Периодическое изменение физического состояния мышечных белков, обусловливающее возможность попеременного сокращения и расслабления мышц и выполнения механической работы, очевидно, каким-то образом связано с важнейшими, дающими энергию химическими процессами. [7]
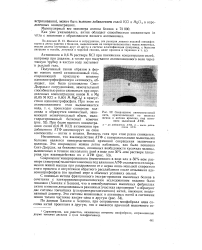 |
Сокращение актомиозиновой нити, приготовленной из миозина щенка и актина кролика, под влиянием мышечной АТФ. [8] |
С помощью метода фракционного экстрагирования мышечных белков в сочетании с электронномикроскопическим исследованием недавно было показано ( Хаксли и Хенсон), что в невозбужденных мышечных фибриллах актин и миозин локализованы в различных участках саркомеров 1 и образуют две системы тончайших ( ультрамикроскопических) нитей, имеющих неодинаковый диаметр. [9]
 |
Схематическое изображение происхождения креатинурии при прогрессирующей мышечной дистрофии ( по Д.Л. Фердману. [10] |
Наряду с изменениями фракционного состава мышечных белков при поражениях мышц наблюдается снижение уровня АТФ и креа-тинфосфата. Например, через 12 дней после денервации содержание АТФ в денервированной икроножной мышце кролика снижается более чем в 2 раза. Отмечаются также снижение АТФазной активности контрактиль-ных белков ( миозина), уменьшение количества имидазолсодержащих ди-пептидов. [11]
Еще не исследована детальная структура мышечных белков - как сократительных, так и регуляторных. Ее изучение является необходимым условием построения подлинной молекулярной теории мышечного сокращения. Очевидно, что необходимо знание как равновесной структуры, так и динамики ее кон-формационных превращений, ответственных в конечном счете за механохимические процессы в мышце. [12]
Начало исследованию химического состава мышц, в частности мышечных белков, было положено работами А. Я. Данилевского и его учеников. [13]
Глюкокортикоиды способствуют развитию мышечной слабости и атрофии скелетной мускулатуры, что связано с усилением распада мышечных белков, а также снижением уровня кальция в крови. Они тормозят рост, развитие и регенерацию костей скелета. Кортизон угнетает продукцию гиалуроновой кислоты и коллагена, тормозит пролиферацию и активность фибробластов. Все это приводит к дистрофии и дряблости кожи, появлению морщин. [14]
При связывании фермента на колонке при рН адсорбции 6 5 в верхней части ионообменника образуется ярко-красное кольцо мышечных белков, а по мере заполнения колонки белком целлюлоза приобретает опаловую, бледную желтизну. Граница раздела между матовой и желтовато-опаловой зонами постепенно продвигается книзу. После подачи на колонку буфера рН 7 9 ( КОН-трицин) красное кольцо мышечных белков начинает постепенно двигаться книзу, разделяясь при этом на несколько отдельных колец и прокрашивая целлюлозу в бледно-розовый цвет. После того как поглощение при 280 нм в элюате снизится до значения 0 1 - 0 2, на колонку подают буфер ( 10 мМ КОН-трицин, рН 7 9), содержащий вместо 3 мМ ацетата натрия 0 5 мМ 3-фосфоглицерат. [15]
Страницы: 1 2 3 4