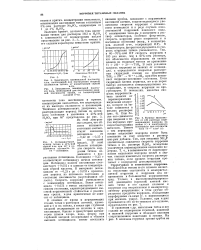
Начало - пассивация
Cтраница 1
Начало пассивации наблюдается при более отрицательных значениях потенциала, тем не менее пассивирующее влияние добавки NO - сказывается в меньшей мере с повышением температуры. [1]
В данном случае критический ток начала пассивации растет с увеличением температуры заметно быстрее, чем ток в пассивной области. [2]
С увеличением скорости обновления поверхности потенциал начала пассивации Е смещается в сторону более положительных значений ( см. рис. 3), соответствующих большей скорости адсорбции кислорода и, следовательно, большей линейной скорости про-движения фронта его адсорбции. [3]
 |
Зависимость минимальной плотности тока, необходимой для наступления анодной пассивности титана, от концентрации серной. [4] |
Потенциал - 0 25 в соответствует потенциалу начала пассивации. Потенциал полной пассивации соответствует 0 052 в и зависит от концентрации серной кислоты. Скорость коррозии уменьшается с повышением потенциала. Выше потенциала 0 052 в титан находится в пассивном состоянии, характеризующемся высокой коррозионной стойкостью в различных средах, к-рая практически не зависит от потенциала. [5]
Потенциал - 0 25 в соответствует потенциалу начала пассивации. Потенциал полной пассивации соответствует 0 052 в и зависит от концентрации серной кислоты. Скорость коррозии уменьшается с повышением потенциала. Выше потенциала 0 052 в титан находится в пассивном состоянии, характеризующемся высокой коррозионной стойкостью в различных средах, к-рая практически не зависит от потенциала. [7]
При потенциалах, более положительных, чем потенциал начала пассивации, скорость адсорбции кислорода уже превышает скорость обновления поверхности. Все большая часть поверхности титанового электрода покрывается хемосорбированным кислородом, вследствие чего сокращается активная поверхность металла и уменьшается плотность анодного тока. Епп, соответствующем минимуму плотности анодного тока, электрод полностью покрыт адсорбированным кислородом. Далее при потенциалах положительнее нуля в пассивной области анодное растворение титана идет с образованием четырехвалентных ионов титана, и для всех скоростей обновления поверхности наблюдается область независимости анодного тока от потенциала. [8]
Для расчета величина А условно приравнивается а критическому току начала пассивации. Тг, количество которых возрастает о температурой. Эти ионы при медленном снятии потенциостатичеокой кривой накапливаются в растворе и путем взаимодействия с иенами 0 оказывают на титан в пассивной области депассивирующее де-лствие, которое также возрастает с температурой. Отметим, что энергия активации процесса растворения титана щш потенциале нахала пассивации составляет 13 7 ккал, а в пассивной области при накоплении ионов Тг3 в растворе - 10 0 кнал и в отсутствие этих ионов - 4 3 наал. [9]
Изменение режима старения влияет на коррозионный потенциал, потенциал начала пассивации, предельную плотность тока и плотность тока полной пассивации. Две последние величины возрастают при переходе структуры от состояния полного отжига к состоянию полного старения. В кислотных средах мартенситно-стареющие стали могут подвергаться и коррозионному растрескиванию. [10]
На диаграмме также имеется вторичная область неполной пассивности между потенциалами начала вторичной пассивации Я и третьим критическим потенциалом Е к, отвечающим полной пассивности при вторичной пассивации. [11]
При потенциалах положительнее точки В становится заметным торможение процесса, связанное с началом пассивации металла. Пассивация обусловлена образованием защитного слоя, который при дальнейшем повышении потенциала ( участок СЯ, так называемая переходная область, падающий участок), вероятно, продолжает распространяться по поверхности электрода. Потенциал максимума тока, который для достаточного развития пассивации должен быть обязательно превышен, часто называют критическим потенциалом пассивации ( фкр), а соответствующую плотность тока ( IKD) - критическим током пассивации. Область Я /, НК или ЯМ, где стационарная скорость растворения невелика ( 10 - 8 - 10 - 5 а / смг) и практически не зависит от потенциала и полностью связана с электрохимическим процессом ( суммарная реакция Me Mem - j - me), называют областью пассивного состояния, или, короче, пассивной областью. Рост скорости ионизации при увеличении потенциала здесь полностью компенсируется одновременно протекающим процессом увеличения количества пассивирующего вещества на поверхности и, возможно, повышением защитных свойств пассивирующего слоя. [12]
 |
Коррозионная стойкость сплавов титана. [13] |
Основными электрохимическими характеристиками, определяющими пассивируемость металла, как отмечалось, являются потенциал начала пассивации У, потенциал полной пассивации Vn. Определив изменение этих характеристик титана при легировании его каким-либо элементом, можно судить о пригодности этого элемента как компонента в коррозионно-стойком сплаве. Таким образом, исследование анодной поляризации потенциостатическим методом и определение зависимостей скорости коррозии от потенциала может служить основой для выбора легирующих компонентов и построения теории коррозионно-стойкого легирования не только применительно к титану, но и к другим металлам, устойчивость которых определяется пассивным состоянием. [14]
Очевидно, константа А по порядку величины должна быть близка к критическому току начала пассивации металла при данной темпера туре. [15]
Страницы: 1 2 3 4