Начало - пассивация
Cтраница 3
Переходный характер области 1 4 - 2 2 в находит отражение и в кинетических измерениях. Торможение проявляется обычно в спаде тока окисления; потенциалы начала пассивации для различных веществ не совпадают. [31]
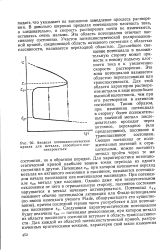 |
Анодная потенциостатическая кривая для металла, способного пассивироваться. [32] |
Для характеристики потенциостатической кривой наиболее важны точки перехода из одного состояния в другое. Потенциал еп, при котором начинается переход металла из активного состояния в пассивное, называется потенциалом начала пассивации или потенциалом пассивации. При потенциале еак металл уже пассивен. Однако даже при незначительном отклонении от него в отрицательную сторону, пассивное состояние нарушается и металл начинает активироваться. Потенциал еак называют обычно потенциалом активации или Фладе-потенциалом ( по имени немецкого ученого Flade, обнаружившего его существование), причем последний термин часто употребляют и для потенциала пассивации еп. Следующим характеристическим потенциалом будет величина вдп - потенциал депассивации, при котором металл из области пассивного состояния вступает в область транспассивности. [33]
Титан и его сплавы подчиняются общим закономерностям перехода из активного состояния в пассивное и обратно, установленным для др. пассивирующихся металлов ( см. Коррозия нержавеющих сталей), Пассивное состояние достигается либо анодной поляризацией, либо добавлением окислителей. Коррозионное поведение титана и его сплавов определяется величиной стационарного потенциала и его расположением по отношению к равновесному потенциалу, потенциалу начала пассивации и потенциалу полной пассивации ( первый критич. Для титана следует различать 2 типичных состояния: активное и пассивное. Склонность титана к пассивации, как и др. металлов и сплавов, может быть охарактеризована значением критич. [34]
Анодные кривые для титана и хрома одинаковы. На кривой можно отметить следующие характерные точки: Vcm - стационарный потенциал, внешний ток равен нулю, Vп - потенциал начала пассивации соответствует максимальному току анодного растворения металла. При потенциалах, более положительных, чем потенциал полной пассивации, металл находится в пассивном состоянии, поддерживаемом внешней анодной поляризацией. Различие в анодном поведении титана и хрома состоит в следующем: при высоких положительных потенциалах пассивное состояние титана не нарушается, в то время как у хрома наступает состояние перепассивации [10-12], в котором он начинает растворяться в виде шестивалентных ионов. Потенциал полной пассивации у хрома более отрицательный, чем у титана. Перенапряжение водорода на хроме несколько более низкое, чем на титане. Поэтому в области потенциалов, где титан активно анодно растворяется на молибдене, протекают катодные процессы. Анодное растворение молибдена наблюдается только при значительном смещении его потенциалов в положительную сторону. Сопоставлением весовых потерь и количества пропущенного электричества установлено как в наших опытах, так и в работе [13], что растворение молибдена происходит в виде шестивалентных ионов. Молибден является кор-розионностойким металлом в серной кислоте. [35]
Увеличение концентрации плавиковой кислоты приводит к заметному расширению области потенциалов активного растворения и к резкому росту тока при всех исследованных потенциалах. Данные, приведенные в таблице, свидетельствуют, что при увеличении концентрации плавиковой кислоты от 1 0 до 3 0 н потенциалы начала пассивации ( р нп) и полной пассивации ( р титана смещаются в положительном направлении почти на 150 мв, а критический ток пассивации возрастает почти в 4 5 раза. [36]
При анодной защите на стали образуется защитная пассивирующая пленка, придающая металлу высокую коррозионную стойкость. Для создания такой пленки необходимо в течение определенного времени анодно поляризовать сталь, причем плотность тока должна быть не меньше плотности тока, соответствующей началу пассивации на анодной кривой. [37]
Результаты исследований коррозионного поведения поверхности железа, ионно-импланти-рованной хромом, показали, что электрохимическое поведение ионно-легированного и объемно-легированного хромом железа мало отличается при близких концентрациях хрома. Как при объемном, так и при поверхностном легировании железа хромом наиболее благоприятно изменяется большинство параметров в сторону повышения пассивности и коррозионной стойкости: потенциалы начала пассивации и полной пассивности смещаются в отрицательном направлении, при этом изменяются предельная плотность тока пассивации и плотность тока полной пассивности. [38]
Он изучил начальную стадию пассивации железа в условиях коррозии при разомкнутой цепи и показал, что изменение толщины пленки от 15 до 20 А связано с началом пассивации. [39]
Одновременное воздействие на повышение анодной пассивируемости и введение в сплав катодных присадок может значительно облегчить пассивируемость сплава и, следовательно, повысить его коррозионную стойкость. Как уже обсуждалось выше ( см. рис. 56, 57, а), большую роль в процессе пассивации сплавов, легированных катодными присадками, играет величина потенциала начала пассивации Еа и потенциала полной пассивации Епп сплава. [40]
Участок АВ характеризует условия активного растворения металла. Здесь с ростом анодного потенциала скорость растворения увеличивается. Точка В соответствует потенциалу начала пассивации. [42]
 |
Поляризационные диаграммы. [43] |
Участок диаграммы АС соответствует активному состоянию металла, когда происходит интенсивное растворение его. При потенциале, большем, чем в точке В, начинается образование защитной пленки, что приводит к увеличению поляризации. Потенциал точки С называется потенциалом начала видимой пассивации. Он соответствует максимальной скорости анодного процесса / а. [44]
Так же, как и в случае межкристаллитной коррозии, металл характеризуется несколькими анодными кривыми, зависящими от адсорбционных свойств поверхности и наличия металлических или неметаллических включений. Точечная и язвенная коррозия особенно характерна в средах, содержащих хлорид -, бромид-или иодид-ионы, которые адсорбируются на отдельных участках металла. Условия пассивации на таких участках резко отличаются от основного фона металла как по потенциалам начала пассивации, так и по потенциалам полной пассивации. Изменяется также величина критического тока пассивации и потенциал пробоя. Точечная и язвенная виды коррозии проявляются или в области потенциалов, характеризующих переход из активного состояния в пассивное, или в области высоких потенциалов, характеризующих переход из пассивного состояния в состояние пробоя. [45]
Страницы: 1 2 3 4
