Отдельные белок
Cтраница 1
Отдельные белки обладают значительным разообразием в аминокислотном составе, химических свойствах, величине молекулярного веса и физиологической роли. Такое же - разнообразие наблюдается и в отношении физико-химических свойств белков. Большинство белков имеет ясно выраженный характер лиофильных коллоидов; в клетках и тканях белки находятся или в состоянии золя, или в состоянии геля. Некоторые белки образуют коллоидные растворы при растворении в воде или в спирте, для других - золеобразование возможно лишь в присутствии электролитов. [1]
Растворимость отдельных белков помимо прочего зависит от их заряда. Механизм высаливающего действия солей при осаждении белка рассмотрен в разд. [2]
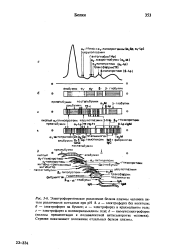 |
Электрофоретическое разделение белков плазмы человека пя. [3] |
Стрелки показывают положение отдельных белков плазмы. [4]
Для определения относительного содержания отдельных белков в саркоплазме используют метод электрофореза на бумаге. Разделение белков основано на различии в подвижности ионов белковых молекул в электрическом поле. Скорость перемещения молекул пропорциональна величине их свободного заряда. Величина заряда молекул различных белков саркоплазмы неодинакова, а поэтому и скорость их перемещения в электрическом поле тоже разная, что дает возможность разделить белки плазмы на несколько фракций. [5]
Подобное различие в поведении отдельных белков говорит о том, что поверхность их глобулярных молекул образована различными молекулярными группами. [6]
Для определения относительного содержания отдельных белков в саркоплазме используют метод электрофореза на бумаге. Разделение белков основано на различии в подвижности ионов белковых молекул в электрическом поле. Скорость перемещения молекул пропорциональна величине их свободного заряда. Величина заряда молекул различных белков саркоплазмы неодинакова, а поэтому и скорость их перемещения в электрическом поле тоже разная, что дает возможность разделить белки плазмы на несколько фракций. [7]
Значительно более трудную задачу представляет количественное определение отдельных белков в природных веществах. Стечением времени удалось разработать ряд методов, в которых использованы и физико-химические свойства белков и осаждение их как нейтральными солями, так и кислотными реагентами. [8]
Число аминокислотных остатков, входящих в макромолекулы отдельных белков, весьма различно: в инсулине их 51, в миоглобине - около 140, в белке ВТМ - свыше 300 тыс. Поэтому и молекулярный вес белков колеблется в очень широких пределах - от 10 000 у. [9]
Читатель может найти в этих обзорах сведения об анализе отдельных белков. В этом методе применен градиентный проявитель-ный анализ на ионообменных колонках из сульфированного полистирола. На рис. 165 показан типичный пример [62] превосходного разделения, осуществленного этим методом. [10]
Условия, при которых происходит осаждение сульфатом аммония, настолько характерны для отдельных белков ( за редкими исключениями), что это свойство можно сравнить с растворимостью, характеризующей кристаллические вещества. [11]
Образование таких комплексов весьма затрудняет изучение растворимости, хотя иногда и облегчает выделение отдельных белков из их смесей. Подобного рода комплексы возникают в том случае, если белок и второй компонент обладают противоположными зарядами в той области рН, которая лежит между их изоэлектрическими точками. Поскольку основным типом связи здесь является электростатическое взаимодействие, то увеличение ионной силы раствора до высоких значений ( до 2 М) приводит к разрушению комплексов. Примерами могут служить инсулинат протамина и дезоксирибонуклео-протеины, образованные ДНК и основными белками ядра - гистонами. [12]
Итак, все многообразие форм жизни на нашей планете обусловлено существованием нескольких миллионов отдельных белков, каждый из которых в своем роде уникален. [13]
Несмотря на небольшой объем, книга Блока п Боллинг пригодна как справочник благодаря наличию многочисленных таблиц аминокислотного состава отдельных белков, целых органов, пищевых веществ. [14]
Ниже излагаются основное общие способы очистки белков, а также примеры того, как разные способы сочетаются в процессе очистки отдельных белков. В заключение рассматриваются критерии полноты очистки белков. [15]
Страницы: 1 2 3 4