Независимость - скорость - реакция
Cтраница 1
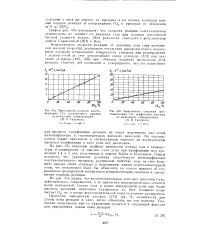 |
Зависимость скорости восстановления СО - графитовой частицы от начальной концентрации ( П. Н. Галушко. [1] |
Независимость скорости реакции от давления газа ( при постоянной весовой скорости) доказывает отсутствие предполагаемого некоторыми авторами отравления поверхности углерода при реагировании с углекислотой за счет хемадсорбции окиси углерода [132] или двуокиси углерода [195, 265] при обычных условиях протекания этой реакции. [2]
Независимость скорости реакции от парциального давления хлористого водорода указывает на необратимость этой стадии. Малая энергия активации ( 9 5 ккал / моль) связана с высокой яуклеофильяосты) амина в электрофильяостью фосгена. Довольно высокая ( - 23 5 кал / моль К) энтропия активации указывает, что образуется активированный комплекс со значительными изменениями геометрии молекул я уменьшением степени свободы. Механизм отличается от предложенного в работе [4], тем, что не предусматривает атаку промежуточного комплекса второй молекулой амина для отщепления хлористого водорода. [3]
Эта независимость скорости реакции от природы вступающей группы характерна не только для инертных комплексов Co ( III), Cr ( III) и Rh ( III), но также для октаэдрических комплексов, по крайней мере для моиоден-татных лигандов. Таким образом, скорость реакций обмена и замощения для лабильных комплексов переходных и непереходных металлов не зависит от природы замещающей группы. Кажущиеся исключения наблюдаются для некоторых хелатообразующих лигандов, но они, вероятно, обусловлены специальным механизмом. Этот вопрос будет обсуждаться позднее. [4]
Наблюдаемая в некоторых случаях независимость скорости реакции от температуры, выражающаяся равенством температурного коэффициента единице, указывает на простоту механизма реакции. [5]
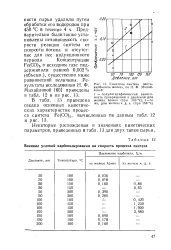 |
Влияние условий карбонилироваиия на скорость процесса синтеза.| Кинетика синтеза пента-карбонила железа, по Н. Ф. Михайловой. [6] |
Предварительно были также установлены независимость скорости реакции синтеза от скорости потока и отсутствие для нее индукционного периода. [7]
 |
Триалкилфосфаты, полученные реакцией триалкилфосфитов. [8] |
На основании кинетических данных и независимости скорости реакции от полярности растворителя был предложен радикальный механизм реакции. [9]
В электрохимических и коррозионных исследованиях участки независимости скорости реакции от потенциала, подобные показанным на рис. II. В таких случаях приходится выяснять природу предельного тока. Увеличение его при перемешивании раствора доказывает связь этого тока с диффузией в растворе, но не является однозначным доказательством того, что он имеет чисто диффузионную природу: как мы уже отметили выше, диффузия может быть лишь одной из замедленных стадий. [10]
Пиридилметильные производные марганца и молибдена также показывгют независимость скорости реакции от концентрации кислоты и анионов; для них предполагается мономолекулярный гомо-лиз связи углерод - металл на основании общих соображений и результатов по ацидолизу соответствующих ртутноорганических соединений. [11]
В отсутствии конкурирующих элементарных процессов должна была бы наблюдаться независимость скорости реакции от диаметра сосуда. Подобное запаздывание во времени или период индукции действительно наблюдался [ 35, 36J; его очень трудно объяснить на основе только чисто гомогенной реакции. Из-за недостатка количественных данных протекание реакции (1.84) в газовой фазе не должно в настоящее время считаться совершенно исключенным. [12]
В отсутствии конкурирующих элементарных процессов должна была бы наблюдаться независимость скорости реакции от диаметра сосуда. Подобное запаздывание во времени или период индукции действительно наблюдался [ 35, 36J; его очень трудно объяснить на основе только чисто гомогенной реакции. Из-за недостатка количественных данных протекание реакции (1.84) в газовой фазе не должно в настоящее время считаться совершенно исключенным. [13]
Эта схема приводит в согласии с экспериментальными данными к независимости скорости реакции от концентрации пропана и кислорода. Для подобной замены имеется, по мнению авторов, еще и то основание, что благодаря ей реакция вместо цепной становится свободно-радикальной, что и наблюдалось при низких температурах. [14]
Авторы полагают, что их схема приводит также к независимости скорости реакции от температуры. Однако среди реакций, включенных в схему, основная реакция образования радикалов С3Н7 ( реакция 4) несомненно связана с энергией активации порядка 8 - 9 ккал / молъ и потому предложенная схема не может считаться удовлетворительно объясняющей и второй экспериментальный факт - независимость скорости от температуры. [15]
Страницы: 1 2 3 4