Независимость - скорость - реакция
Cтраница 2
Эта реакция характеризуется первым порядком по катиону диазония и независимостью скорости реакции от концентрации воды как нуклеофильноо агента. Кроме того, скорость реакции не изменяется при зауне ЩО на D2O в качестве нуклеофильного агента. Добавки других нуклеофилов ( кроме воды) приводят к смеси продуктов, но не влияют на скорость. [16]
Эта реакция характеризуется первым порядком по катиону диазония и независимостью скорости реакции от концентрации воды как нуклеофильного агента. Кроме того, скорость реакции не изменяется при замене Н2О на D2O в качестве нуклеофильного реагента. Добавки других нуклеофилов ( кроме воды) приводят к смеси продуктов, но не влияют на скорость. Отсутствие обмена водорода на дейтерий для солей диазония ArN2 в среде D2O исключает образование дегидробензола в качестве интермедиата. Малая селективность по отношению к различным нуклеофилам в конкурирующих реакциях свидетельствует о высокой активности интермедиата и согласуется с образованием арил-катиона в качестве такого интермедиата. [17]
Так, в работе [135] авторы исследуют химический процесс, предполагая независимость скорости реакции от концентрации кислорода и температуры, что - ни в коей мере не соответствует действительности. Более строго сформулирована модель в работах [136, 137], однако и здесь сделаны необоснованные допущения и не проведено Исследование решения. [18]
Так, в работе [11] автор исследует химический процесс, предполагая независимость скорости реакции от концентрации кислорода и температуры, что ни в коей мере не соответствует действительности. [19]
При низких температурах реагирования в опытах Рида и Уилера может быть отмечена независимость скорости реакции от линейных скоростей дутьевого потока. Однако развитие при этих температурах реакции окисления окиси углерода затрудняет возможность исследования кинетических характеристик первичного процесса. [20]
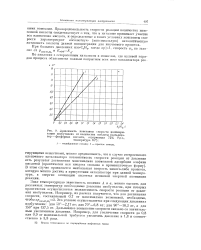
Обычным критерием того обстоятельства, что диффузия не является процессом, определяющим скорость реакции, является независимость скорости реакции от степени перемешивания. Так, для проверки условий, при которых можно определить истинные скорости окисления, Джордж, Райдил и Робертсон [14] исследовали влияние скорости встряхивания на скорость поглощения кислорода тетралином. Экспериментальные данные для 1 г вещества при 108 приведены на рис. 4, на котором кривая А соответствует некатализированной реакции, а кривые Б и В-реакциям в присутствии ускорителей. Низкие скорости реакции в случае А совершенно не зависят от встряхивания, в то же время более высокие скорости в случае В повышаются при увеличении скорости встряхивания. [21]
Образование в фотохимических реакциях горячих частиц с их повышенной реакционной способностью, в частности, проявляется в независимости скорости реакции от температуры. [22]
Справедливость квазирезонансной гипотезы может быть экспериментально проверена различными методами, в основе которых лежит одна идея - независимость скорости реакции от характера возбуждения и ее зависимость только от плотности энергетических состояний молекулы. [23]
Образование в фотохимических реакциях горячих частиц с их повышенной реакционной способностью, в частности, проявляется в независимости скорости реакции от температуры. Так, например, обстоит дело с изученной Шф льтцем и Тейлором [504] реакцией образования метана при фотолизе CH3J излучением ртутной линии 2537 А. [24]
 |
Зависимость константы скорости полимери. [25] |
Зная температурную зависимость величин А и а, можно оцепить для различных температур необходимые давления изобутилена, при которых практически осуществляется независимость скорости реакции от давления изобутилена. Это условие осуществляется при следующих давлениях изобутилена: для 50 - 2 17 ат; для 70 - 6 8 ат; для 90 - 18 3 ат, а для 150 при 137 5 ат. Дальнейшее повышение скорости связано со значительным увеличением давления. Например, для увеличения скорости до 0 8 или 0 9 от максимальной требуется увеличить давление в 1 8 и соответственно в 3 8 раза. [26]
Заменяя 6А выражением изотермы Лэнгмюра, мы, в предельных случаях, получаем либо пропорциональность скорости реакции первой степени объемной концентрации вещества А, либо независимость скорости реакции от объемной концентрации вещества А. [27]
Как будет видно из дальнейшего, многие реакции имеют третий порядок, часто встречается дробный порядок реакции и даже нулевой ( по одному из компонентов), что означает независимость скорости реакции от концентрации одного из взаимодействующих веществ. Наблюдаются явления катализа и ингибирования ( отрицательного катализа) - ускорения или соответственно замедления реакции компонентом, концентрация которого не изменяется по ходу реакции. Распространены также процессы автокатализа реакции ее же продуктами, в результате чего скорость реакции до определенного предела возрастает по мере расходования исходных компонентов, а не уменьшается, как у других типов реакции. В системах, близких к термодинамически равновесным, начинает играть заметную роль реакция, обратная основной. [28]
В обоих случаях в полимерной цепи будет содержаться незначительное количество NH2 - rpynn, но в любом случае, предположение французских исследователей [3] о том, что только обрыв цепи происходит с участием радикалов NH2, не согласуется с данными о независимости скорости реакции от концентрации аммиака. [29]
Скорость процесса ограничивается в основном скоростью диффузии хлора к поверхности реакции. Независимость скорости реакции от температуры вплоть до 700 С вызвана постоянством диффузионной проницаемости прохлорированного слоя. Выше 800 С нелетучие хлориды частично выплавляются. Повышение текучести этого расплава приводит, вероятно, к его перераспределению по внутренней поверхности брикета и к изменению пористости слоя. Скорость диффузии хлора с повышением температуры увеличивается, но это компенсируется повышением хлорируемости концентрата. [30]
Страницы: 1 2 3 4