Независимость - скорость - реакция
Cтраница 3
Более хорошо согласуется с полученным материалом предположение о том, что реакция протекает между адсорбированным бензолом и раство-ренным в палладия водородом. Тогда полученная независимость скорости реакции от концентраций бензола и водорода в газовой фазе становится понятной. В этом случае скорость реакции должна быть пропорциональна поверхностной концентрации бензола и объемной концентрации ЕЬ в палладии, которые могут быть независимы друг от друга. [31]
По полученным результатам строят зависимость скорости реакции от скорости подачи газа или от числа оборотов мешалки. Область независимости скорости реакции от условий мас-сообмена соответствует кинетической. Внутри этого интервала выбирают скорость подачи газа или число обороток мешалки и фи-ксир уют это значение во всех последующих кинетических экспериментах. [32]
Наблюдаемая в некоторых случаях независимость скорости реакции от температуры, выражающаяся равенством температурного коэффициента единице, указывает на простоту механизма реакции. Действительно, обращаясь к механизму наиболее подробно изученной реакции разложения йодистого водорода, приведенному на стр. [33]
При изучении кинетических закономерностей реакции очень важно обеспечить хорошее перемешивание: скорость процесса должна определяться скоростью реак ции ( кинетическая область), а не скоростью растворения газа. Для кинетической области характерна независимость скорости реакции от интенсивности перемешивания. [34]
При изучении кинетических закономерностей реакции очень важно обеспечить хорошее перемешивание: скорость процесса должна определяться скоростью реакции ( кинетическая область), а не скоростью растворения газа. Для кинетической области характерна независимость скорости реакции от интенсивности перемешивания. [35]
Хотя доказательств недостаточно, по-видимому, эти скорости действительно представляют собой скорости для ионных пар, практически полностью образующихся в растворе. Если так, то существует поразительная независимость скорости реакции от природы присутствующего в растворе аниона. Это несколько удивительно, так как из рис. 3.8 видно, что нитро-группа должна способствовать механизму 3 2 или по крайней мере требует образования связи более сильной в переходном состоянии. Если ионная пара не участвует в реакции, то скорость определяющей ступенью, вероятно, будет образование сольвато-комплекса, который затем реагирует более быстро с образованием замещенного комплекса. [36]
В ряде предыдущих опытов, например, Джонстона, Чена и Скотта [278], также установлен рост внутренней поверхности угля по мере протекания реакции. Большая роль внутреннего реагирования подтверждается независимостью скорости реакции от размера частиц в интервале 14 и 18, 25 и 36, 52 и 72 отверстий ситовой пробы по британскому стандарту. [37]
Ацетильный комплекс III образуется в присутствии монооксида углерода и быстро взаимодействует с ним при низком давлении, что согласуется с независимостью скорости карбонили-рования от парциального давления монооксида углерода. Участием метилиодида в образовании этих промежуточных соединений объясняется независимость скорости реакции от концентрации метанола. Первый порядок реакции по родию и иоду позволяет предположить, что лимитирующей стадией реакции карбонилирования метанола является присоединение метилиодида к аниону дииододикарбонилродия. Как уже говорилось, ИК-спектр раствора катализатора, записанный в условиях реакции при повышенной температуре, показал наличие в растворе только аниона [ Rh ( CO) 2l2 ] - - По-видимому, стадии, следующие за окислительным присоединением метилиодида, протекают очень быстро. Это подтверждает вывод, что лимитирующей стадией реакции является окислительное присоединение метилиодида. [38]
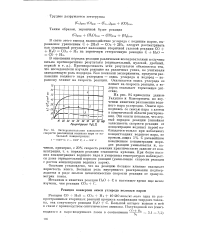 |
Экспериментальная зависимость. [39] |
Опытами установлено, что на реакцию большое влияние оказывает пористость кокса. Большая роль внутреннего реагирования подтверждается в ряде опытов независимостью скорости реакции от гранулометрии кокса. [40]
Для такого механизма замещающая группа не играет существенной роли в образовании переходного состояния и, следовательно, не оказывает влияния на скорость полной реакции. Характерная особенность большинства реакций замещения октаэдрических комплексов состоит в независимости скорости реакции от природы замещающей группы. [41]
Простейший метод определения коэффициента эффективности сводится к измерению скорости реакции на гранулах нескольких размеров в одинаковых условиях. Признаком того, что т) - 1 является независимость скорости реакции, отнесенной к единице массы катализатора, от размера гранул. При этом значение коэффициента эффективности для более крупных частиц равно отношению удельных скоростей реакции на крупных и тонкоизмельченных частицах. [42]
Анализ системы ( 6) был проведен в работе 4, где получены критерии, позволяющие определить лимитирующую стадию процесса. В частности, признаком протекания реакции в кинетической области является независимость скорости реакции от характеристических размеров образца. [43]
Анализ системы ( 6) был проведен в работе 4Э, где получены критерии, позволяющие определить лимитирующую стадию процесса. В частности, признаком протекания реакции в кинетической области является независимость скорости реакции от характеристических размеров образца. [44]
Однако, как показали Раис и Герцфельд [1063], вследствие двоякого действия стенок, возможны такие случаи, когда, несмотря на наличие гетерогенных стадий реакции, ее скорость не будет зависеть от величины 5: V. Таким образом, мы должны заключить, что рассматриваемый метод дает однозначное указание о влиянии гетерогенного фактора на течение реакции лишь в тех случаях, когда скорость реакции оказывается зависящей от величины отношения поверхности стенок реакционного сосуда к его объему. При независимости скорости реакции от величины 5: У; заключение о том, что реакция на всех ее стадиях протекает р гомогенной ( газовой) фазе, не всегда может быть правильным, и следовательно, решение вопроса о влиянии гетерогенного фактора на реакцию требует дополнительного исследования. [45]
Страницы: 1 2 3 4