Sd-орбита
Cтраница 1
Sd-орбитами атома кремния обладают свойствами кислот, заметно более сильных, чем их органические аналоги - спирты. [1]
 |
Электронные конфигурации переходных элементов четвертого периода. [2] |
Возможно существование Sd-орбит с более или менее одинаковой энергией. Поэтому для перехода к следующему, более высокому уровню энергии необходимо сначала разместить десять электронов на пяти 3d - орбитах. Не только скандий, но и следующие девять элементов строятся путем размещения электронов на Sd-орбитах. И только с элемента с порядковым номером 31 - галлия - начинают заполняться орбиты с более высокой энергией. [3]
Строгая направленность Sd-орбит в CaV2O6 следует из сопоставления электрических свойств со спектрами ЭПР. Электропроводность этого ванадата описывается теорией Мотта, согласно которой ее определяют два процесса: туннели-рование на относительно большие расстояния и термоактивированные перескоки на ближайшие свободные состояния. [4]
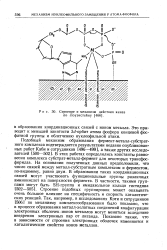 |
Строение и механизм действия киназ по Лоуэнстейну. [5] |
Это приводит к меньшей занятости Sd-орбит атома фосфора концевой фосфатной группы и облегчению нуклеофильной атаки. [6]
Замещение водорода на иод объясняют взаимодействием Sd-орбиты фосфора и электронов В - Н, в результате которого атомы водорода становятся менее электроотрицательными, чем атом бора. [7]
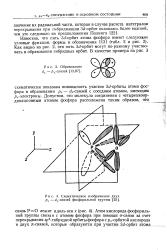 |
Образование d - р - связей.| Схематическое изображение двух р - d - связей фосфорильной группы. [8] |
Как видно из рис. 2, эти пять Sd-орбит могут по-разному участвовать в образовании гибридных орбит. [9]
Так, существенно, что в кремнии есть Sd-орбиты, близкие по энергии, к 5Р3 - гибридному состоянию, вследствие чего кремний может быть акцептором электронов на свои d - орбиты. Благодаря этим особенностям в кварцевом стекле при введении в него различных добавок может происходить существенное перераспределение электронов, ответственных за химическую связь, что приводит к изменению степени ионности связей в стекле. [10]
Однако вполне возможно, что в некоторых соединениях на вакантные Sd-орбиты атома фосфора могут внедряться неподеленные пары электронов атомов, непосредственно не связанных с фосфором, е образованием циклических структур. [11]
Авторы полагают, что это связано с наличием л-взаимо-действия между заполненными Sd-орбитами Вг и 5р - и гибридной 5s 5р - орбитами рения. [12]
При последовательном добавлении электронов с переходом к другим элементам электроны занимают Sd-орбиты, пока не будут заняты все десять мест на этих орбитах. [13]
Характерной общей особенностью атомов фосфора и серы является наличие у этих элементов вакантных Sd-орбит, которые могут участвовать в сопряжении с заместителями. В переходном состоянии в нециклических соединениях сопряжение может быть более выраженным, что приведет к большей стабилизации молекулы. В переходном состоянии в пятичленных циклических эфирах фосфорной и серной кислот наличие дополнительных я-связей в связях Р - О и S - О должно приводить к еще более выраженному напряжению в циклической системе по сравнению с тем, как это предполагалось ранее [172] только за счет деформации угла в переходном состоянии. С другой стороны, жесткость кольца может привести к тому, что сопряжение фосфора и серы с кислородом циклических эфирных группировок будет проявляться в меньшей степени, чем в открытых эфирах. Следовательно, d - р - сопряже-ние заместителей с Sd-орбитами атома серы или фосфора, влияющее на стабильность переходного состояния, по-разному проявляется в циклических и нециклических эфирах, что, по-видимому, является основной причиной более высокой реакционной способности циклических эфиров и более высоких значений теплоты реакции. [14]
Таким образом, изложенные в настоящем разделе некоторые квантовомеханические представления о роли Sd-орбит элементов третьего периода в гибридизации электронных оболочек, а также результаты спектральных методов исследования соединений с че-тырехкоординационным атомом фосфора в основном состоянии молекулы и другие вышеприведенные данные свидетельствуют о возможности образования я-связей между заместителями у фосфора и тетраэдрическим атомом фосфора с использованием 3 -орбит последнего. Изменение степени л-связанности фосфорильной группы коррелирует со сдвигом частот инфракрасных и ультрафиолетовых спектров поглощения этой группы при изменении положительного заряда на атоме фосфора в зависимости от индуктивного влияния заместителей, хотя результаты исследований по ультрафиолетовым спектрам свидетельствуют о возможности сопряжения других заместителей с Зс. В то же время данные ЯМР довольно четко подтвердили наличие подобного PTI - й - сопряжения. Анализ полученных данных свидетельствует о том, что передача электронных влияний заместителей, особенно эффекта сопряжения, через фосфорильную группу в производных кислот тетраэдрического фосфора значительно менее выражена, чем в производных карбоновых кислот. [15]
Страницы: 1 2 3 4