Sd-орбита
Cтраница 4
Вообще создается впечатление, что если по соседству с атомом фосфора находится элемент третьего периода ( S, СГ), то снижается возможность участия в сопряжении с реакционным центром неподеленной пары электронов этих гетероатомов, в результате чего облегчается нуклеофильная атака на тетраэдрический атом фосфора и повышается реакционная способность фосфорсодержащих соединений. Вопрос о том, почему неподеленные пары электронов элементов третьего периода в значительно меньшей степени участвуют в сопряжении с Sd-орбитами атома фосфора, чем электроны элементов второго периода ( О, F), довольно сложен, и можно лишь отметить, что, по-видимому, определенную роль играют большие межатомные расстояния и наличие у элементов третьего периода своих d - орбит. [46]
Для переходных металлов характерно наличие свободных d - орбит, на которых обычно и располагаются электроны присоединяющихся групп. Однако это не необходимое условие, так как, например, Zn2 является очень хорошим комплексообразователем, несмотря на то что все его Sd-орбиты заполнены. Для образования комплексов могут использоваться и другие орбиты с достаточно низкой энергией. [47]
Тетракарбонил никеля имеет тетраэдрическую конфигурацию. Но это не ведет к парамагнетизму, так как нейтральный атом никеля имеет на два электрона больше, чем двухвалентный никель, и Sd-орбиты полностью заняты парами. СО) 4 диамагнитен так же, как и все другие карбонилы металлов и родственные вещества [ в том числе Со ( СО) зМО, Fe ( CO) 2 ( NO) 2) Fe ( CO) 5) Fe2 ( CO) 9, Fe3 ( CO) 12) Cr ( CO) 6, Mo ( CO) 6 ], магнетизм которых изучен. [48]
Однако, как следует из данных табл. 7, возможность участия заместителей в сопряжении с атомом фосфора в данной работе не вызывает сомнения. То, что этот вывод не соответствует результатам исследований инфракрасных и ультрафиолетовых спектров поглощения, а также спектров комбинационного рассеяния, авторы [87 ] объясняют особенностями строения тетраэдрической молекулы и симметрии Sd-орбит. [49]
Ионный радиус мало изменяется при переходе от одного элемента к другому. В значительной степени причиной этого является равновесие двух эффектов: 1) с возрастанием заряда ядра электроны должны притягиваться сильнее, поэтому размеры ионов должны уменьшаться; 2) по мере заполнения Sd-орбит число электронов возрастает, поэтому они должны отталкиваться друг от друга, т.е. размеры ионов должны увеличиваться. Эти два эффекта взаимно компенсируют друг друга. Для одного и того же заряда ядра отрыв каждого З - электрона уменьшает отталкивание между остальными Зй-электронами, что позволяет им приблизиться к ядру. [50]
Элемент с порядковым номером 21 должен иметь на один электрон больше. На первый взгляд, можно было бы ожидать, что двадцать первый электрон займет 4р - орбиту как следующий за 4в - орбитой более высокий уровень энергии Но между 4s - и 4р - орбитами, находятся пять Sd-орбит, которым соответствуют значения энергии, промежуточные между 4s - и 4р - уровнями. [51]
Рассмотренные в настоящем разделе данные о ферментативных реакциях с участием биологически важных фосфорилирующих агентов находятся в соответствии с современными представлениями о механизме нуклеофильного замещения у тетраэдрического атома фосфора. Из этих данных следует, что той аналогии, которая иногда допускается в трактовке механизмов ферментативных реакций, связанных с нуклеофильным замещением у атома углерода карбонильной группы в производных карбоновых кислот и нуклеофильным замещением у тетраэдрического атома фосфора, быть не может. Важная роль Sd-орбит атома фосфора и р - - сопряжения заместителей, связанных с фосфором в переходном состоянии при нуклеофильном замещении у атома фосфора, из рассмотренного материала вполне очевидна. Дальнейшее исследование этого вопроса может привести к лучшему пониманию зависимости между строением, реакционной способностью и физиологической активностью некоторых фосфорсодержащих соединений, а также к новым интересным данным в области энзимологии, в частности к дальнейшему изучению природы макроэргических связей. [52]
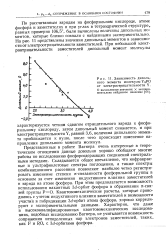 |
Зависимость дипольного момента молекулы Y3PO от электроотрицательности Y. О вычисленное значение. X экспериментально найденное значение. [53] |
Представленные в работе Вагнера очень интересные в теоретическом отношении данные довольно хорошо обобщают многие работы по исследованию фосфорсодержащих соединений спектральными методами. Складывается общее впечатление, что инфракрасные и ультрафиолетовые спектры поглощения, а также спектры комбинационного рассеяния позволяют наиболее четко регистрировать изменение степени я-связанности фосфорильной группы в основном за счет изменения индуктивного влияния заместителей и заряда на атоме фосфора. При этом предполагается возможность использования вакантных Sd-орбит фосфора в образовании л-свя-зей группы РО. Квантовомеханические расчеты, которые проводились с учетом индуктивного влияния заместителей и возможности участия в гибридизации Sd-орбит атома фосфора, хорошо коррелируют с экспериментальными данными. Характерно, что даже в высококвалифицированных квантовомеханических исследованиях, подобных исследованию Вагнера, не учитывается возможность сопряжения неподеленных пар электронов заместителей, таких, как F и RO, с З - орбитами фосфора. [54]
Страницы: 1 2 3 4