Бензальанилин
Cтраница 2
К 30 г бензальанилина прибавляют 4 5 г анилида диэтилфосфористой кислоты. При этом наблюдается разогревание реакционной смеси. После охлаждения вся масса закристаллизовывается. [16]
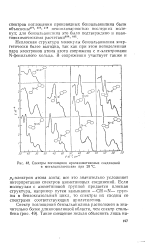 |
Спектры поглощения арилазометиновых соединений в метилциклогексане при 20 С. [17] |
Неплоская структура молекулы бензальанилина энергетически более выгодна, так как при этом неподеленная пара электронов атома азота сопряжена с зт-электронами N-фенильного кольца. [18]
Бром присоединяется к бензальанилину ( I) при обработке его в хло-роформенном растворе хлороформекпым же раствором брома. [19]
В отличие от молекулы бензальанилина, связь CN которой способствует неплоской конфигурации молекулы, молекула бензоксазола плоская благодаря наличию кислородного мостика. Неподеленная пара электронов атома кислорода взаимодействует с л-электронами атома азота, заметно повышая энергию пл - уровней, так что они уже не сказываются на спектрально-люминесцентных свойствах молекул. [20]
Например, 20 г бензальанилина СеНв СН: NCeHs растворяют в 100 г абсолютного спирта, нагревают с 10 г натрия в течение 1 часа на водяной бане и осаждают бензиланилин С НВ - СНа NH СеНв водой. [21]
По этой схеме с бензальанилином легко конденсируются ацетон, метилэтилкетон, метилизобутилкетон, метил-н. [22]
По этой схеме с бензальанилином легко конденсируются ацетон, метилэтилкетон, метилизобутилкетон, метил-н. [23]
Отметим интересную реакцию метилкетонов с бензальанилином в присутствии BF3, которая была изучена Снайдером, Корнбергом и Ромигом [120] и является простым методом получения ( З - аминокетонов. [24]
Если нагреть фенил-глиоксиловую кислоту с бензальанилином, например, до 137, то наблюдается выделение двуокиси углерода. [25]
Если нагревать фенилглиоксиловую кислоту с бензальанилином, то кетокислота расщепляется не в любом количестве, как следовало бы ожидать, а 1 моль бензаль-анилина приводит к выделению самое большее 3 молей двуокиси углерода. Следовательно, во время реакции катализатор расходуется. [26]
Берут по 10 ммо-лей диазоацетона и бензальанилина в бензоле ( 100 мл) и, применяя аппаратуру для введения вещества по каплям, проводят реакцию. Бензол удаляют испарением в вакууме, остаток, растворенный в бензоле, подвергают хроматогра-фическому разделению. Бледно-желтый элюат снова упаривают, а остаток смешивают с небольшим количеством метанола. Добавляя к маточному раствору воду и охлаждая, можно получить еще 0 5 г вещества с низкой ( 60) температурой плавления. Из него перекристаллизацией из метанола выделяют еще 0 20 г р-лактама. [27]
Аналогичная ситуация наблюдается для стильбена, бензальанилина и глиоксаля, для которых расчет неправильно предсказывает устойчивость молекулярной конформации с взаимно ортогональными я-системами. [28]
Уменьшение сопряжения у 9-антральанилина по сравнению с бензальанилином может быть вызвано не только уже отмеченными, но и другими стерическими факторами. [29]
Например, бензилидентрифенилфосфоран превращается в бензаль-дегид через стадию бензальанилина. [30]
Страницы: 1 2 3 4