Равновесная жидкость
Cтраница 1
Равновесная жидкость, судя по координатам треугольника, оказывается состоящей из 20 / 0 А, 60 / 0 В и 20 / 0 С. [1]
Равновесную жидкость промывают водой или раствором бикарбоната. Затем отгоняют растворители, воду, циклические и низкомолекулярные полимеры для получения продукта с низкой летучестью и высокой температурой вспышки. Обычно фракционирование силиконов вязкостью 20 ест и более проводят в вакууме ( 1 - 5 мм рт. ст.) при 300 С. Силиконовая жидкость должна быть нейтральной, так как в этом случае она обладает лучшей стабильностью. [2]
Составы равновесных жидкости и пара образуют бинодаль, аналогичную бинодали растворимости в тройных системах. [3]
 |
Диаграмма давление пара - состав раство-ра при положительном отклонении от закона Рауля с максимумом давления ( 1 и при отрицательном отклонении с минимумом давления ( 2. [4] |
На различии составов равновесных жидкостей и пара осно - ван метод разделения растворов на компоненты, называемый перегонкой. [5]
При понижении темп-ры состав равновесных жидкости и кристаллов меняется. Вновь выпадающие из сплава т при 1 кристаллы уже имеют состав / г, а прежде выпавшие кристаллы посредством диффузии выравнивают свой состав с новыми. [6]
Здесь Ср - теплоемкость термодинамически равновесной жидкости; Ср - теплоемкость при замороженной реакции ( IX. Иными словами, Ср представляет собой теплоемкость жидкости, в которой не происходит перестроек структуры. При температурах, более низких, чем температура стеклования глицерина Tg - - 185 К, теплоемкости кристаллами, стекла практически совпадают. Экстраполируя этот результат в область температур Т Те, получаем Ср - Сярист. Величина 8СР СР - Ср, как видно из рис. 55, практически не зависит от температуры. [7]
Первый из них связывает составы равновесных жидкости и пара и влияние добавок компонентов на общее давление пара. Согласно этому закону увеличение относительного содержания данного компонента в жидкой фазе всегда вызывает увеличение относительного содержания его в парах. Пар по сравнению с находящейся с ним в равновесии бинарной жидкостью относительно богаче тем из компонентов, прибавление которого в системе повышает общее давление пара или понижает температуру кипения смеси при данном давлении. [8]
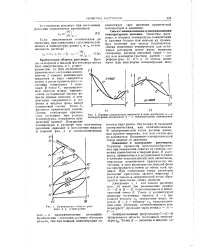 |
Кривые равновесных жидкости и пара растворов. а - с температурным минимумом. б - с температурным максимумом. [9] |
При достижении критического состояния компонентом 2 кривые равновесных жидкости и пара смещаются влево, а после критического состояния компонента 1 исчезают. В точке С, промежуточной области между критиче скими состояниями чистых веществ кривые кипения и конденсации соединяются, и паровая и жидкая фазы имеют одинаковый состав. Точка С, является критической точкой. Линия, огибающая критические состояния при разных температурах, называется критической кривой. [10]
Первый закон Коновалова характеризует соотношения между составами равновесных жидкости и пара и влияние добавления того или другого из компонентов на общее давление пара. [11]
Предложена новая рациональная форма аналитического представления плотности равновесных жидкости и пара и данных по давлению насыщения чистых веществ, основанная на представлении экспериментальных данных в специальной системе координат. Предлагаемый подход использован для обработки экспериментальных данных по двуокиси углерода. [12]
В методе Редлиха-Кистера проверяют данные по составам равновесных жидкости и пара, в расчет вводят еще отношение давлений пара чистых компонентов. Точность же измерений давления пара раствора ( или температуры кипения) на результаты проверки не влияют. [13]
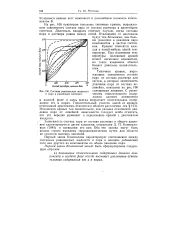 |
Составы равновесных жидкости сплошными линиями. С увели-и пара в различных системах. чением относительного содер. [14] |
Первый закон Коновалова характеризует соотношения между составами равновесных жидкости и пара и влияние добавления того или другого из компонентов на общее давление пара. [15]
Страницы: 1 2 3 4