Равновесная жидкость
Cтраница 2
Между этими кривыми заключена гетерогенная область, состоящая из равновесных жидкости и пара. Чем дальше отстоят друг от друга равновесные кривые, тем больше различие в составе пара и жидкости и тем проще протекает процесс перегонки. [16]
Условия ( 65) будут выполняться, когда состав равновесных жидкости и пара одинаковы. Таким образом, к числу особых точек будут относиться точки концентрационного комплекса, соответствующие компонентам и азеотропам. [17]
Это разделение протекает тем легче, чем больше различие составов равновесных жидкости и пара. С; равновесному составу пара отвечает точка /: пар более, чем раствор, богат пентаном; поэтому остаю-щийся. [18]
В настоящей работе предлагается один из возможных вариантов рационального аналитического представления плотности равновесных жидкости и пара и давления насыщенных чистых веществ. [19]
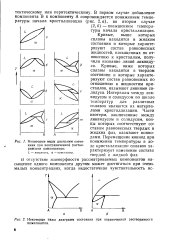 |
Некоторые виды диаграмм состояния при неограниченной растворимости компонентов.| Некоторые виды диаграмм состояния при ограниченной растворимости компонентов. [20] |
Кривые, выше которых сплавы находятся в жидком состоянии и которые характеризуют состав равновесных жидкостей, насыщенных по отношению к кристаллам, получили название линий ликвидуса. Кривые, ниже которых сплавы находятся в твердом состоянии и которые характеризуют состав равновесных по отношению к жидкостям кристаллов, называют линиями со-лидуса. Интервалы между ликвидусом и солидусом по шкале температур для различных сплавов являются их интервалами кристаллизации. Части изотерм, заключенные между ликвидусом и солидусом, концы которых соответствуют составам равновесных твердых и жидких фаз, называют конно-дами. [21]
 |
Баротропное явление в бинарной системе. [22] |
При дальнейшем сжатии количество жидкости будет увеличиваться по правилу рычага, а составы равновесных жидкости и пара будут двигаться навстречу друг другу по бинодали. Например, когда фигуративная точка системы достигнет точки е, жидкость будет иметь состав, соответствующий точке q, а газ - точке q - i. [23]
Мембранный потенциал может быть легко обнаружен с помощью двух каломельных электродов, помещенных в равновесные жидкости, находящиеся по обе стороны от мембраны. В случае положительно заряженного коллоида, потенциал каломельного электрода, погруженного в камеру с коллоидом I, всегда оказывается более положительным, чем потенциал каломельного электрода, опущенного в равновесный раствор, не содержащий коллоида. [24]
Другая особенность метода Редлиха-Кистера состоит в том, что проверяют соответствие данных о составах равновесных жидкости и пара и данных о давлении пара чистых жидкостей, правильность же данных о давлении пара ( температуре кипения) растворов не находит отражения в результатах, так как рассматриваются отношения коэффициентов активности двух компонентов. Это обстоятельство вызывает двойственную оценку. С одной стороны, это некоторое ограничение метода, проверяют не всю совокупность величин, характеризующих равновесие. Но в этом же можно видеть и преимущество метода - проверяют составы равновесных фаз, именно тех характеристик равновесия, которые наиболее важны в практическом отношении, в частности, для расчета ректификации. [25]
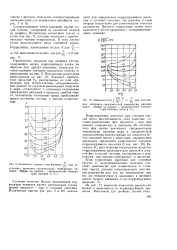 |
Показатель степени п как функция - - при постоянных значениях среднемольной температуры кипения. ( Цифры на кривых - среднемольные температуры кипения в С. [26] |
Значения критических давлений Ph, рассчитанные по этой корреляции при использовании экспериментальных данных по составам равновесных жидкости и пара, согласуются с опытными величинами критических давлений в пределах ошибки опыта; исключение составляют смеси, приближающиеся по своему составу к чистым компонентам. [27]
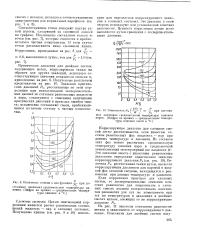 |
Показатель степени п как функция - - при постоянных значениях среднемольной температуры кипения. ( Цифры на кривых - среднемольные температуры кипения в С. [28] |
Значения критических давлений РЬ, рассчитанные по этой корреляции при использовании экспериментальных данных по составам равновесных жидкости и пара, согласуются с опытными величинами критических давлений в пределах ошибки опыта; исключение составляют смеси, приближающиеся по своему составу к чистым компонентам. [29]
 |
Прибор Бушмакина. [30] |
Страницы: 1 2 3 4