Бензамид
Cтраница 2
Как бензамид реагирует со следующими соединениями: а) Н2О ( Н), t; б) Вг2, КОН; в) LiA. [16]
Гидропизуют бензамид и образующуюся кислоту этерифицируют фенолом, используя в качестве агента конденсации трифторуксусный ангидрид. [17]
Получение бензамида [ 60 % из 1 2-дибензоилгидразина и никеля Ренея W-2 ( гл, 4 Спирты, разд. [18]
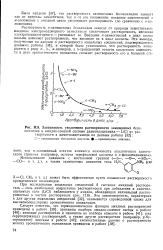 |
Зависимость увеличения растворимости замещенных бензанилидов в амидно-солевой системе диметилацетамид - LiCl от растворимости в диметилацетамиде по данным работы. [19] |
Растворимость я-замещенных бензамидов зависит от природы заместителей: введение электронодонорного заместителя увеличивает растворимость, введение электроноакцепторного - уменьшает ее. Введение га-заместителей в цикл амина меньше изменяет растворимость, чем введение их в цикл кислоты. [20]
По охлаждении выпавший бензамид отфильтровывают, отжимают и перекристаллизовывают из воды. [21]
На примере бензамида схема ( 172) показано, что в качестве интермедиата образуется имидоилхлорид. Вместе с тем оказалось, что формамиды и некоторые алкиламиды практически не активны в этой реакции. В результате термического распада имидоилхло-рида стадия ( б) на схеме ( 172) образуются бензонитрил и ал-килгалогенид. Реакция служит удобным препаративным методом превращения алифатических аминов в соответствующие алкил-галогениды. Первое направление включает гетеролиз N-алкильной связи по механизму, подобному 5 1, с последующим быстрым выбросом хлорид-иона. Второе направление осуществляется в обратной последовательности, а именно после первоначального отщепления хлорид-иона образуется ион нитрилия, который далее взаимодействует с хлорид-ионом по механизму подобному Sw2, и эта стадиячопределяет скорость процесса. Если R1 ароматическая группа, то преобладает процесс Sw2 - THna, так как промежуточно образующийся карбениевый ион стабилизуется за счет резонанса. [22]
При реакции бензамида с фенилтетрахлорфосфором в обычных условиях образующееся фосфазосоединение полностью распадается на бензонитрил и дихлорангидрид фенилфосфоновой кислоты. При проведении реакции в вакууме получается смесь бензонитрила, дихлорангидрида фенилфосфоновой кислоты и фе-нилдихлорфосфазобензоила, разделить которую очень трудно. [23]
В виде бензамидов удалось эффективно разделить алифатические амины, причем применение радиоизотопного метода обеспечило высокую точность определения. [24]
Был выделен также бензамид. [25]
Во избежание образования бензамида необходимо удалить аммиак полностью. [26]
Был выделен также - бензамид. [27]
Ю-6), а бензамид в нитробензоле вообще почти не проводит, раствор обоих веществ в том же раствори. Бензамид и бром дают соединение состава C6H6NH2 - Br2, известное даже в твердом состоянии. [28]
Такие соединения, как бензамид, очень легко гидролизуются и требуется большое внимание, чтобы не принять их за вещества кислотного характера. [29]
Систематические исследования алкиламидов, бензамидов и анилидов показывают, что кислотно-катализируемый гидролиз гораздо более чувствителен к стерическому, чем к электронному влиянию заместителей. Это согласуется с обоими направлениями, представленными на схеме ( 126), так как в обоих случаях необходима регибридизация sp2 - - sp3 карбонильного атома углерода. Первичные амиды, как правило, более реакционноспособны, чем вторичные и третичные в силу стерических эффектов. Данные по алкиламидам, собранные в работе [218], указывают на хорошую корреляцию скоростей реакции с модифицированным уравнением Тафта, содержащим члены, характеризующие стерические и гипер-конъюгационные, но не полярные, взаимодействия. Поскольку скорость кислотного гидролиза в большинстве случаев не зависит от структуры, наиболее важным параметром с синтетической точки зрения является максимум скорости. Это означает, что не всегда самым эффективным будет использование наиболее концентрированной кислой среды, так как, грубо говоря, максимальная скорость будет достигаться в том растворе, для которого значение Яд приблизительно равно р / Са амида. [30]
Страницы: 1 2 3 4