Неравноценность - связь
Cтраница 3
Вывод о неравноценности связей в молекуле азота подтверждается тем, что энергия их разрыва различна. [31]
 |
Схема перекрывания 2р - электроняы. облаков в молекуле N2. а - о-связь. б и в - п-связи. [32] |
Вывод о неравноценности связей в молекуле азота подтверждается тем, что энергия их разрыва различна. [33]
Рассматривая направление перегруппировки несилш-диметилди-фенилэтиленгликоля, можно вывести заключение, что большей способностью к отщеплению обладает та гидроксильная группа, которая находится у углеродного атома, связанного с фенилами. Тиффено объяснил такую неравноценность связи гидроксильных групп, исходя из представлений Вернера о переменной валентности, и ввел понятие о сродспгвоемкосгтш радикалов. Он считал, что чем больше сродствоемкость радикала, тем больше сродства на связь с ним затрачивает соединенный с этим радикалом углеродный атом и тем меньше у этого атома остается сродства на связь с гидроксилом. Путем изучения пинаколиновых перегруппировок многих несимметричных пи-наконов, содержащих попарно сравниваемые группы, были составлены ряды радикалов, расположенных в порядке убывания сродст-воемкости; эти ряды использовали в течение двух десятилетий при разрешении различных теоретических проблем. [34]
Рассматривая направление перегруппировки несыл-диметилди фениленгликоля, можно вывести заключение, что большей спосоС ностью к отщеплению обладает та гидроксильная группа, котора находится у углеродного атома, связанного с фенилами. Тиффен объяснил такую неравноценность связи гидроксильных групп, ис ходя из представлений Вернера о переменной валентности, и вве. Он считал, что чем больш сродствоемкость радикала, тем больше сродства на связь с ним за трачивает соединенный С этим радикалом углеродный атом и те. Путем изучения пинаколиновых перегруппировок многих несиммет ричных пинаконов, содержащих попарно сравниваемые группы, быт составлены ряды радикалов, расположенных в порядке убываню сродствоемкости; эти ряды использовали в течение двух десяти лети i при разрешении различных теоретических проблем. В настоящее вре мя имеются более четкие представления электронной теории. Согласно этим представлениям преимущественное течение процесса при пинаколиновой перегруппировке только в одном направлении обусловливается различной склонностью к диссоциации по связи QQ; изомерных оксониевых соединений ( стр. [35]
Расстояния Мотетр-О в тетраэдрах, так же как и в октаэдрах, не вполне равноценны. Естественной причиной этого является неравноценность связей О-Моокт, сопряженных с МотеТр - О. Локализация электронной плотности на отдельных связях в октаэдрах вызывает индукционный эффект и в сопутствующих полиэдрах. Однако в целом они значительно меньше искажений в октаэдрах. Средние параметры тетраэдров во всех трех структурах очень близки. [36]
В первом из этих соединений существующая в принципе неравноценность связей Мо - N нитрил и Мо-ГЧамин не сказывается па межатомных расстояниях: все три расстояния Мо-Ок одинаково укорочены ( 1 736 и 1 739 А), все три расстояния Мо-N одинаково удлинены ( 2 32 и 2 33 А) по сравнению с характерными для ординарных связей. [37]
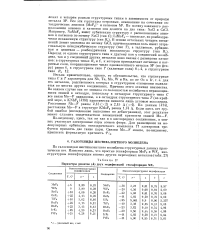 |
Параметры решеток ( А двух модификаций гексафторидов MFe. [38] |
Причина этого отличия неизвестна. Во всяком случае она не связана со склонностью молибдена к неравноценности связей в октаэдре, поскольку в октаэдрах структурного типа С все связи Мо-F одинаковы, а в октаэдрах структурного типа Т ( по крайней мере, в KNbFe [478]) практически имеются лишь угловые искажения. По данным [474], расстояния Мо-F в структуре KMoF6 равны 1 74 А. [39]
Все фильтраты и неиспользованные активные растворы по окончании работы сливают в специальную бутыль для слива отходов. Данные опыта заносят в таблицу ( форма 9) и на основании полученных результатов делают заключение о равноценности или неравноценности связей в комплексном иодиде ртути. [40]
Подобные комплексы, согласно Яцимирскому [131], называются внешнесферными. В щелочной среде из комплексов типа Ln2L образуются гидроксокомплексы, при этом один эквивалент металла выпадает в виде гидроокиси, что служит дополнительным подтверждением неравноценности связи катионов, входящих в полиядерные комплексы. [41]
Новые заместители вступают в нафталиновое кольцо только в определенные положения по отношению к уже имеющимся заместителям. Правила ориентации в нафталиновом кольце аналогичны правилам ориентации в бензольном кольце, однако имеются и специфические черты, связанные с наличием второго кольца и более выраженной неравноценностью связей. [42]
Второй важной особенностью нафталина является неравноценность его ароматических связей. В то время как в бензоле и его производных все ароматические связи имеют одинаковый порядок, в нафталине выравненность связей нарушена: связи 1 - 2, 3 - 4, 5 - 6 и 7 - 8 имеют более высокий порядок, более непредельны, а связи 2 - 3 и 6 - 7 - более низкий порядок, меньшую электронную плотность, чем связи бензола. Неравноценность связей нафталина проявляется во многих особенностях его реакционной способности. [43]
 |
Схема перекрывания 2р - электронных облаков в молекуле N2. в - ( Т - связь. б я в-я-связи. [44] |
Как показывает рис. 35, атомы азота связаны в молекуле N2 тремя ковалентными связями. Вывод о неравноценности связей в молекуле азота подтверждается тем, что энергия их разрыва различна. [45]
Страницы: 1 2 3 4