Sd-подуровень
Cтраница 2
Электроны заполняют 4 / -, а не Sd-подуровень потому, что в этом случае они обладают меньшей энергией. [16]
С элемента скандия ( Z21) начинается заполнение Sd-подуровня, так как он энергетически более выгоден, чем 4р - подуро-вень. В атомах последующих элементов вплоть до инертного элемента криптона ( Z36) идет заполнение 4р - подуровня. [17]
В атомах каких элементов происходит проскок электрона с 4s - на Sd-подуровень. [18]
Четвертый период начинается с калия, в атоме которого остается свободным Sd-подуровень, но наружный электрон располагается на энергетически более выгодной 45-орбитали. У калия на ней находится один электрон, а у кальция - два. [19]
Для электронного строения никеля ( 3d84s2) характерна близость к завершению Sd-подуровня. Это делает Sd-подуровень никеля ( 3d8) более стабильным, чем в случае кобальта ( 3d7) и особенно железа ( 3d6), Поэтому, хотя переход Ni / Ni2 характеризуется величиной Е0 0 23 В. Поэтому трехвалентное состояние никеля маловероятно: Ni ( III) должен, проявлять свойства сильнейшего окислителя и стабилизация его является трудной задачей. [20]
 |
ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ ( по Некрасову. [21] |
От Hf ( 72) до Hg ( 80) продолжается заполнение Sd-подуровня. Элементы Т1 ( 81) - Ru ( 86) очередные электроны направят в бр-подуровень. [22]
У цезия начинается постройка шестой оболочки, хотя не только не образовался еще Sd-подуровень на пятой оболочке, но и на четвертой еще не начиналась постройка 4 / - подуровня. Заполнение этого подуровня, находящегося уже глубоко внутри атома, происходит только у элементов от Се ( 2 58) до Lu ( Z 71), составляющих группу редкоземельных элементов, или лантаноидов. Атомы этих элементов обладают аналогичной структурой двух наружных оболочек, но различаются по степени достройки внутренней ( четвертой) оболочки. Эти элементы весьма мало различаются между собой по химическим свойствам, так как химические свойства определяются главным образом структурой наружных электронных оболочек. Подобный же случай встречается еще раз в седьмом периоде периодической системы. У элементов, следующих за актинием и называемых актиноидами, происходит достройка / подуровня пятой оболочки. [23]
У цезия начинается постройка шестой оболочки, хотя не только не образовался еще Sd-подуровень на пятой оболочке, но и на четвертой еще не начиналась постройка 4 / - подуровня. Заполнение этого подуровня, находящегося уже глубоко внутри атома, происходит только у элементов от Се ( Z 58) до Lu ( Z 71), составляющих группу редкоземельных элементов, или лантаноидов. Атомы этих элементов обладают аналогичной структурой двух наружных оболочек, но различаются по степени достройки внутренней ( четвертой) оболочки. Эти элементы весьма мало различаются между собой по химическим свойствам, так как химические свойства определяются главным образом структурой наружных электронных оболочек. Подобный же случай встречается еще раз в седьмом периоде периодической системы. У элементов, следующих за актинием и называемых актиноидами, происходит достройка f подуровня пятой оболочки. [24]
У следующих после кальция десяти элементов, начиная со скандия, происходит формирование Sd-подуровня. [25]
 |
Некоторые свойства атомов платиновых металлов. [26] |
Как видно из табл. 34, у атомов платиновых металлов достраивается 4d - или Sd-подуровень. [27]
Как видно из табл. 39, у атомов платиновых металлов достраивается Ы - или Sd-подуровень. [28]
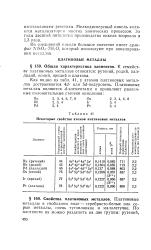 |
Некоторые свойства атомов платиновых металлов. [29] |
Как видно из табл. 41, у атомов платиновых металлов достраивается 4d - или Sd-подуровень. [30]
Страницы: 1 2 3 4