Бензоат-ион
Cтраница 1
Бензоат-ион в течение всего процесса остается тесно связанным с катионом, причем если проводить перегруппировку в присутствии других ионов, то последние не входят в продукт перегруппировки. [1]
Бензоат-ион в водных растворах бесцветен, подвергается гидролизу, способен к образованию бен-зоатных комплексов металлов. [2]
Для осаждения бензоат-ионов используют перхлорат ртути. Вследствие некоторой растворимости осадка бензоата ртути излом кондуктометрической кривой в точке - эквивалентности закруглен. [3]
При аналогичной реакции бензоат-ионов с сульфатом меди ( П) выделяется осадок бирюзового цвета. [4]
К смеси, полученной после открытия бензоат-иона, прибавляют 1 мл хлороформа, подкисляют несколькими каплями серной кислоты, прибавляют еще 2 - 3 капли крепкого раствора хлорида железа ( III) и взбалтывают; хлороформ окрашивается в янтарно-желтый цвет. [5]
Таким образом только 0 14 % от исходной концентрации бензоат-иона реагирует с водой с образованием бензойной кислоты, и наши расчеты заслуживают доверие. [6]
В результате описанных опытов можно сделать вывод, что защитное действие бензоат-ионов при рН5 5 обусловлено образованием на металле поверхностной пленки нерастворимого комплексного соединения, которая препятствует переходу ионов металла в раствор. [7]
 |
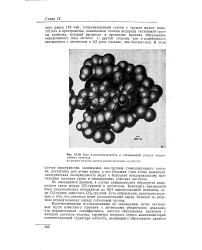
Модели Полинга - Кори - Колтуна для комплекса а-циклогекса. [8] |
Следовательно, реакция идет в две стадии, и образование льнитрофенола предшествует образованию бензоат-иона. [9]
 |
Исправленные времена удерживания ( мин анионов в. [10] |
Таким образом, увеличение концентрации аниона А - в элюенте равно уменьшению концентрации бензоат-иона. [11]
 |
Ион n - азосукцинанилата и связывающий участок гомологичного антитела. На рисунке показана высокая комплементарность их структур. [12] |
С другой стороны, ион п-хлорбензоата связывается с антителом в 3 5 раза сильнее, чем бензоат-ион. [13]
С О) при 1690 см 1 и появления пиков симметричного и асимметричного колебаний ( СОО -) бензоат-иона при 1425 и 1555 см 1 авторы работы [19] заключили, что бензальдегид хемосорбирован на окиси алюминия в виде бензоат-иона. [14]
В системе тритилбензоата, например, константа скорости перемешивания 180 (3.159) & приблизительно в 40 раз выше, чем константа скорости обмена с меченым бензоат-ионом. Либрация Х - в ионной паре, которая вызывает перемешивание метки ( 3.162 а), протекает быстрее, чем вращение R ( 3.162 6), - таков разумный вывод наличия других данных о стерических затруднениях, создаваемых такому вращению. [15]
Страницы: 1 2 3 4