Исходное нитросоединение
Cтраница 3
Первый служит исходным материалом для получения о-аннзп-дииа, который имеет значение как диазосоставляющая красителе. Для красочной промышленности о-нитроанизол особенно важен как исходное нитросоединение в синтезе дианнзидина ( см. гл. Моноамины, отвечающие двум последним нитроэфпрам ( III и IV), применяются как диазо-тпрующиеся основания в холодном крашении по азотолам. [31]
В целом ряде производств получения мономеров определяющим технологическим узлом является восстановление различных ароматических нитросоединении, синтезированных на предыдущих стадиях процесса. В качестве восстанавливающего агента используется водород, исходное нитросоединение - в жидкости, а реакция протекает на твердом катализаторе. В технологически оправданных растворителях ( их доступность, простота переработки катализата и т.п.) исходное нитросоедине-ние, как правило, слабо растворимо, и в реакторе вместе с катализатором суспендированы частички исходного реагента. [32]
Полинитропроизводные ароматических углеводородов вступают во взаимодействие с сульфитом натрия уже при весьма низких ( до - 100 С) температурах, образуя хорошо растворимые в воде яркоокрашенные соединения. При под - - кислении указанных растворов регенерируется исходное нитросоединение. [33]
Можно предположить, что взаимодействие нитрозосоединения с арилгидроксиламином, катализируемое щелочью, является той основной реакцией, в результате которой в растворе может происходить образование азок-сисоединения. Однако Лукашевичем [33] была показана возможность образования азоксисоединения при взаимодействии исходного нитросоединения с арилгидроксиламином. Обе эти реакции обусловливают накопление в щелочном растворе азоксисоединения. Само по себе азоксисоединение обладает достаточной реакционной способностью. [34]
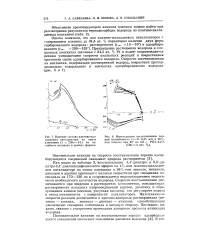
Как видно из таблицы 3, восстановление 4 4 -динитро - и 3 3 -ди-нитро - 4 4 -диаминодифенилового эфиров на 4 % - ном платино-палладие-вом катализаторе на окиси алюминия в 96 % - ном этаноле, метаноле, диоксане и ацетоне протекает с малыми скоростями при смещениях потенциала на 170 - 220 мв и сопровождается недопоглощением теоретически необходимого количества водорода. Скорости восстановления увеличиваются при введении в растворитель компонентов, повышающих растворимость исходных нитросоединений ( ацетон, диоксан), и образующихся аминов ( аммиак, уксусная кислота), что регулирует подвод и отвод компонентов с поверхности катализаторов. Максимальные скорости реакции достигаются в протоно-донорных растворителях ( метанол - аммиак, метанол - диоксан - аммиак), способствующих увеличению смещения потенциала в анодную сторону. Последнее, видимо, связано с ускорением протекания донорного процесса активации водорода. [36]
Конечным продуктом восстановления не всегда является амино -: оединение. В зависимости от выбранного восстановителя и условий зосстановления одно и то же исходное нитросоединение может дать различные продукты восстановления. [37]
По мере повышения плотности тока растет потенциал катода, и при определенном значении потенциала выход алкилгидроксиламина начинает падать в результате дальнейшего его восстановления в амин. Катодная плотность тока, при которой падает выход алкилгидроксиламинов, существенно зависит от природы катода, исходного нитросоединения, температуры и других условий электролиза. [38]
Образующиеся в щелочной среде в присутствии камфоры при обратимом одноэлектронном восстановлении ароматических нитросоединений анион-радикалы способны химически окисляться находящимися в растворе окислителями [ JO, тартрат меди ( П) ] до исходных нитросоединений, которые вновь восстанавливаются на электроде, давая дополнительный, кинетически ограниченный ток. Анион-радикалы способны также вступать в реакцию дисмутации, в результате которой образуется соответствующее производное гидроксиламина и регенерируется исходное нитросоединение [119]; восстановление последнего на капельном электроде обусловливает появление дополнительного - по отношению к высоте одноэлектронной волны - кинетического тока, так что суммарная волна может достигать даже уровня 4 ( или 6) - электронного перехода, отвечающего полному восстановлению нитросоединения. [39]
Образующиеся в щелочной среде в присутствии камфоры при обратимом одноэлектронном восстановлении ароматических нитросоединений анион-радикалы способны химически окисляться находящимися в растворе окислителями [ JO, тартрат ] меди ( П) ] до исходных нитросоединений, которые вновь восстанавливаются на электроде, давая дополнительный, кинетически ограниченный ток. Анион-радикалы способны также вступать в реакцию дисмутации, в результате которой образуется соответствующее производное гидроксиламина и регенерируется исходное нитросоединение [119]; восстановление последнего на капельном электроде обусловливает появление дополнительного - по отношению к высоте одноэлектронной волны - кинетического тока, так что суммарная волна может достигать даже уровня 4 ( или 6) - электронного перехода, отвечающего полному восстановлению нитросоединения. [40]
Как правило, суммарный выход продуктов электровосстановления и по току и по веществу мало зависит от концентрации нитросоединения в исходном растворе. Однако соотношение между выходами двух продуктов электролиза - гидроксиламина и амина - существенно меняется в зависимости от содержания исходного нитросоединения в электролите. [41]
Нитроновые кислоты, представляющие собой аци-форму нитросоединений, являются весьма нестойкими веществами. Большинство из них - относительно слабые кислоты с рКа 2 - 6, и в этом отношении они проявляют сходство с карбоновыми кислотами, но в отличие от последних их химические свойства тесно связаны со свойствами стабильной таутомерной формы - исходных нитросоединений. [42]
При жидкофазном гидрировании через жидкую реакционную массу, находящуюся в контакте с твердым катализатором, барбо-тируют водород. Для увеличения скорости процесса его почти всегда ведут под давлением водорода. Исходные нитросоединения вводят в реакцию в виде растворов в органических растворителях или в воде, а иногда в виде водных эмульсий. Это облегчает отвод тепла реакции и выделение продуктов восстановления, которые необходимо отделять от катализатора. Свойства растворителя существенно влияют на скорость процесса гидрирования. Обычно она максимальна в спиртах и в воде и резко падает, если растворитель - ароматическое соединение, диметилформамид и другие. Это объясняется сорбцией таких растворителей активными центрами катализатора. [43]
Существенное влияние оказывает также рН электролита. Например, при восстановлении нитробензола в щелочном электролите в качестве конечного продукта получается не анилин, а фенилгидроксиламин. Кроме того, от рН зависит направление вторичных чисто химических реакций, протекающих между продуктами восстановления и исходным нитросоединением. [44]
Существенное влияние оказывает также рН электролита. Например, при восстановлении нитробензола в щелочном электролите образуется не анилин, а фенилгидроксиламин. Однако, от рН зависит и направление вторичных чисто химических реакций, протекающих между продуктами восстановления и исходным нитросоединением. [45]
Страницы: 1 2 3 4