Углеродный носитель
Cтраница 1
Углеродный носитель оказывает существенное влияние на поведение платинового катализатора. При этом морфология осадка изменяется незначительно, о чем свидетельствует сохранение отношения высот пиков прочно-и слабосвязанного адсорбированного водорода. Специальное исследования показали [18, 91], что уменьшение поверхности платины не связано с ее отравлением или растворением с переходом в объем раствора. Снижение поверхности проявляется в уменьшении числа кристаллитов платины малого размера и роста за их счет более крупных кристаллов. [1]
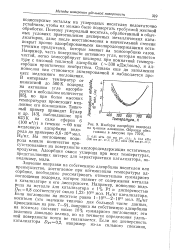 |
Изобары адсорбции водорода. [2] |
Поэтому углеродный носитель, обработанный в обычных условиях приготовления дисперсных металлических катализаторов, даже после восстановления в значительной степени покрыт прочно адсорбированными кислородсодержащими остаточными продуктами, которые влияют на хемосорбцию газов. Например, часть поверхности активного угля, которая является чистой, легко хемосорбирует кислород при комнатной температуре с высокой теплотой адсорбции ( - 330 кДж / моль), и адсорбция практически необратима. Однако еще до заполнения монослоя она становится активированной и наблюдается процесс медленного поглощения. [3]
 |
Поляризационные кривые окисления метанола при 60 С. [4] |
Природа углеродного носителя, по данным ряда работ, оказывает существенное влияние на электрокаталитическую активность микроосадков благородных металлов. В работе [58] наблюдалось увеличение удельной активности микроосадка платины в реакциях электроокисления водорода и электровосстановления кислорода при возрастании поверхности носителя от 700 до 1600 м2 / г. При этом платина, осажденная на уголь, покрытый щелочными оксидами, значительно более активна по сравнению с катализатором, сформированном на угле, покрытом кислыми оксидами. Наибольшей активностью [59] обладает платина на саже XC - 72R с удельной поверхностью - 250 м2 / г и на печной саже с удельной поверхностью - 100 м2 / г. Поверхностные свойства обоих исходных углеродных материалов характеризуются рН, близким к нейтральному. [5]
Большинство активированных углеродных носителей, в частности древесный уголь, имеют развитую пористую структуру и значительную удельную поверхность. Однако они не обладают молекулярно-ситовыми свойствами, так как размер их пор слишком велик и неоднороден. [6]
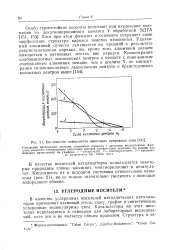 |
Кислотность поверхности некоторых природных глин. [7] |
В качестве углеродных носителей металлических катализаторов применяют активный уголь, сажу, графит и синтетические углеродные молекулярные сита. Катализаторы на этих носителях используются в основном для лабораторных исследований, хотя это и не является общим правилом. [8]
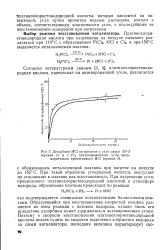 |
Десорбция НС1 во времени с угля марки АР-3 ( кривая / и с 1 / о платинированного угля, предварительно пропитанного НС1 ( кривая У. [9] |
При такой обработке углеродный носитель выступает по отношению к платине как восстановитель. [10]
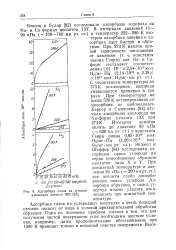 |
Адсорбция газов на т - окиси алюминия дэвисон 992. [11] |
Адсорбция газов на углеродных носителях в очень большой степени зависит от вида и условий предварительной обработки образцов. Одна из основных проблем состоит в том, что для получения чистой поверхности угля необходимы жесткие условия, например, даже продолжительное обезгаживание при 1300 К приводит только к неполной очистке поверхности. [12]
Электропроводность систем шпинель - углеродный носитель, изготовленных в оптимальных условиях, возрастает на два-три порядка по сравнению с чистыми оксидами, а энергия активации проводимости уменьшается на порядок. [13]
Таким образом, эффект углеродного носителя не связан с более широкими возможностями варьирования его удельной поверхности по сравнению с A 20g, а обусловлен, вероятно, спецификой взаимодействия активных компонентов с. [14]
Энергия взаимодействия металлов с углеродными носителями, вероятно, выше, чем с окисными носителями. Так, по данным измерения температурного коэффициента зародышеоб-разования кристаллитов серебра на графите, эта энергия составляет около 92 кДж / моль [70], что соответствует химическому взаимодействию. Бетцольд [5, 40] исследовал методом молекулярных орбиталей системы серебро и палладий на графите и нашел, что энергия взаимодействия значительна; более того, она максимальна в расчете на один атом для одиночного атома металла и уменьшается с увеличением размера агрегата. Согласно результатам этих исследований, из-за сильного взаимодействия с углеродом двумерные агрегаты из шести атомов палладия, находящиеся на поверхности углеродного носителя, не должны иметь rf - зонной структуры. [15]
Страницы: 1 2 3 4