Нуклео-фил
Cтраница 3
Аллильные катионы содержат два центра с недостатком электронов, к которым могут присоединиться нуклео-филы; поэтому при сольволизе аллильных субстратов можно ожидать ал-лильной перегруппировки. Вопрос о молекулярных перегруппировках будет рассмотрен более полно в гл. [31]
Аллильные катионы содержат два центра с недостатком электронов, к которым могут присоединиться нуклео-филы; поэтому при сольволизе аллильных субстратов можно ожидать ал-лильной перегруппировки. Вопрос о молекулярных перегруппировках будет рассмотрен более полно в гл. [32]
Поскольку арсониевые илиды являются лишь особой формой карбаниона, они должны реагировать как типичные нуклео-филы. Сейферс и Коэн [23] подтвердили это, показав, что метилентрифениларсенан ( V) может алкилироваться триметил-бромсиланом. Этот же илид реагирует с эфиратом трехфтори-стого бора, образуя бетаин. Несмеянов и др. [21] установили, что фенацилидентрифениларсенан реагирует как с бромом, так и с серным ангидридом, как типичный нуклеофил, подобно фосфониевым илидам. [33]
Реакция (4.4) несколько более сложная, поскольку образование продукта требует двух последовательных атак нуклео-фила. [34]
Поскольку реакции нуклеофильного замещения в принципе обратимы, отщепившийся заместитель может играть роль нуклео-фила в обратной реакции: поэтому его тенденция к отщеплению должна была бы быть обратно пропорциональна нуклеофильности. В частности, диазониевая группа, является одной из наиболее легко уходящих групп вследствие того, что отщепляющийся элементарный азот обладает очень малой нуклеофильностью. [35]
Хлорфенол, по сравнению с этиловым спиртом, является значительно более сильным электрофилом и менее сильным нуклео-филом. Поэтому в процессе замещения хлора в указанном / - хлориде функцию нуклеофила выполняет молекула этилового спирта, а ж-хлорфенол, образуя водородную связь с анионом хлора, оказывает электрофильное содействие его отщеплению. [36]
Аналогично г) 3-аллильным производным, комплексы палладия с координирующими диенами реагируют с большим числом нуклео-филов. [37]
Если в аллильном положении молекулы имеется уходящая группа, способная реагировать по механизму SNI, то нуклео-фил вместо а-положения может атаковать у-положение. Такой механизм называется SNJ; он был продемонстрирован на примере 2-бутен - 1-ола и З - бутен-2 - ола. [38]
Каждая из стадий этого превращения обратима, и поэтому карбонильное соединение может быть регенерировано при повышении концентрации нуклео-фила ( воды), который будет присоединяться к протонированному оксиму, фенилгидразону, гидразону или семикарбазону, если молекуле будет сообщена энергия, равная энергии, выделяющейся при отщеплении воды. Другими словами, регенерация осуществляется при нагревании до кипения с разбавленной минеральной кислотой. [39]
Аз связь Аз-X ( X На1, ОК, ОАзК2, МК2) легко расщепляется при действии нуклео-филов, связь Аз - Н - в электроф. [40]
В основе этой связи лежит представление о плоской структуре свободного карбониевого иона, который при рекомбинации с любым нуклео-филом будет давать рацемический продукт. [41]
В 1957 г. было показано [32], что имидазол участвует в межмолекулярных реакциях со сложными эфирами в качестве нуклео-фила, причем механизм процесса определяется соотношением ос-новностей атакующей и уходящей групп. [42]
В этих реакциях фосфинистые кислоты проявляют себя как электрофилы, в то время как в других превращениях - как нуклео-филы. [43]
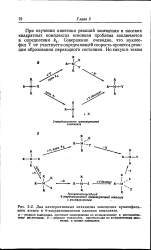 |
Два альтернативных механизма замещения нуклеофиль-ного агента в 4-координационном плоском комплексе. [44] |
При изучении кинетики реакций замещения в плоских квадратных комплексах основная проблема заключается в определении kv Совершенно очевидно, что нуклео-фил Y не участвует в определяющей скорость процесса реакции образования переходного состояния. [45]
Страницы: 1 2 3 4