Область - пассивация
Cтраница 4
Поскольку и феррит, и аустенит пассивируются в растворах щелочей даже очень высоких концентраций, причины растрескивания в этом случае следует искать, очевидно, в смещении потенциала пробоя в отрицательную сторону и вызванном в связи с этим уменьшении величины области пассивации при возрастании концентрации щелочи. [46]
Особенно реальной стала возможность использования и усовершенствования всех подобных методов защиты в 50 - 60 - е годы, когда при помощи потенциостатического метода была полностью изучена зависимость скорости анодной реакции от потенциала как в области активного растворения, так и в области пассивации и перепассивации. [47]
Особенно реальной стала возможность использования и усовершенствования всех подобных методов защиты в 50 - 60 - е годы, когда при помощи потенциостатического метода была полностью изучена зависимость скорости анодной реакции от потенциала как в области активного растворения, так и в области пассивации и перепассивации. [48]
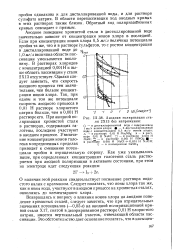 |
Анодная поляризация стали 2X13 без напряжения. [49] |
Возвращаясь к вопросу о влиянии ионов хлора на анодное поведение хромистых сталей, следует заметить, что при отрицательных значениях потенциалов ( - 0 05 в) на анодной поляризационной кривой стали Х17, снятой в деаэрированном растворе 0 01 Н хлористого натрия, имеется вертикальный участок, отвечающий области пассивации. [50]
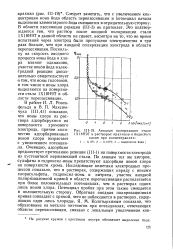 |
Анодная поляризация стали 1Х18Н9Т в растворах крахмала и йодистого. [51] |
Следует заметить, что с увеличением концентрации иона йода область перепассивации и потенциал начала выделения элементарного йода смещаются в отрицательную сторону. В области пассивации реакция ( II1 - 3) не протекает. Это подтверждается тем, что раствор после анодной поляризации стали 1Х18Н9Т в данной области не синеет, несмотря на то, что во время испытаний через электрод было пропущено электричества в три раза больше, чем при анодной поляризации электрода в области перепассивации. Поскольку на скорость анодного процесса ионы йода и хлора влияют одинаково, участие ионОв йода в электродной реакции дополнительно свидетельствует о том, что ионы галогенов, в том числе и ионы хлора выделяются на поверхности стали 1Х18Н9Т в области перепассивации. [52]
При нормальном растворении ( участок АВ поляризационной кривой на рисунке 86, а) анод становится шероховатым, растравленным, покрытым шламом, остатками нерастворившегося металла. В области пассивации ( участки ВС н CD поляризационных кривых) при соответствующем составе электролита достигается полирующий эффект - поверхность металла становится гладкой, глянцевой. Полирование происходит в условиях, когда пассивная пленка тонка; она не прекращает растворение металла, а лишь создает дополнительный потенциальный барьер. В этих условиях выход катионов из кристаллической решетки перестает определяться их положением в ней, а становится следствием случайного появления в пленке на границе с металлом катионных вакансий, что и приводит к равномерному растворению металла. [53]
Положительнее - j - 1 10 в наступает перепассивация хрома. Характерная для области пассивации зависимость скорости реакции от времени в этом случае отсутствует. [54]
Скорость растворения металла резко падает ( отрезок ВС), возникает пассивация металла. Далее отмечается область устойчивой пассивации, характеризующейся практической независимостью плотности тока от потенциала ( отрезок CD), и, наконец, при некотором значении потенциала ( точка D) начинается разряд ионов ОН - или молекул воды. [55]
Исследовано влияние комплексующих добавок роданид -, окоа-лат-ионов и тиомочевины в электролитах на коррозионное поведение образцов. Установлено уменьшение области пассивации, отмечена специфика анодного поведения ВТ - и МДО-образпов. [56]
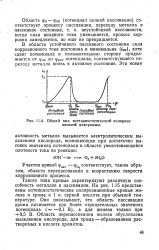 |
Общий вид потенциостатической поляризационной диаграммы. [57] |
Такого типа кривые характеризуют различную способность металлов к пассивации. Они показывают, что область пассивации хрома начинается при более отрицательных значениях, потенциала ( - - 0 1 - В), а для железа только при - j - 0 5 В. [58]
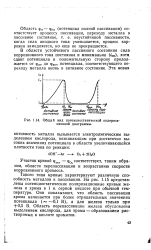 |
Общий вид потенциостатической поляризационной диаграммы. [59] |
Такого типа кривые характеризуют различную способность металлов к пассивации. Они показывают, что область пассивации хрома начинается при более отрицательных значениях потенциала ( - - 0 1 В), а для железа только при 0 5 В. [60]
Страницы: 1 2 3 4 5