Обработка - цеолит
Cтраница 1
Обработка цеолита кислородом сопровождается образованием физически адсорбированных молекул С02 и поверхностных карбонатов. Окись углерода прочно адсорбируется цеолитом Ni Y, и удалить ее можно только вакууми-рованием при 200 С. Частота валентных колебаний связи С - О при адсорбции на Ni - цеолитах на 29 см-1 ниже, чем на цеолитах с катионами Ni2, по-видимому, из-за того, что связь углерода с кислородом на Ni - цеолитах ослаблена. [1]
 |
И К-спектры адсорбированной окиси углерода. [2] |
Обработка цеолита водородом при 150 С приводит к тому, что основная масса катионов восстанавливается до металлического состояния. В спектре наблюдается еще одна полоса - при 1680 см-1, приписанная образованию нитрата. [3]
Обработка цеолитов с катионами переходных металлов восстановительными средами приводит к восстановлению катионов до нульвалентного состояния без нарушения кристаллической структуры цеолитов. Цеолиты в такой форме являются активными катализаторами процессов гидропереработки отдельных органических соединений и нефтяных фракций. [4]
Обработка цеолитов водой подавляет перераспределение водорода между спиртом и кетоном тем сильнее, чем ниже катионная плотность катализатора. При поочередной подаче доз смеси спирта с кетоном и доз воды каталитическая активность изменяется скачкообразно, что объяснено миграцией молекул воды в цеолите. Вода, образующаяся при дегидратации спиртов, оказывает более сильное отравляющее действие, чем подаваемая в виде пара. [5]
Обработка цеолита CuY-A в Н2 ( 400, 0 5 ч), как было показано выше, приводит к восстановлению части катионов меди и образованию центров Си из координационно-ненасыщенных ионов Си2; из сильных магнитных ассоциатов должны образовываться центры типа Си Си, представляющие собой соседние однозарядные ионы меди. [6]
После обработки цеолита кислородом при 360 С выделяется вода. [7]
После обработки цеолита аммиаком полосы поглощения при 3630 и 3540 см 1, характерные для декатионированного цеолита, исчезают, а в области 3350 - 2940 см - появляются довые полосы. Все они, кроме плеча при 3311 и полос при 3184 и 3067 см 1, слабо разрешены. Вид спектров плохо согласуется с присутствием в цеолите ионов аммония или физически адсорбированных молекул аммиака. [8]
После обработки цеолита H2S, S или SO2, а затем кислородом увеличивается способность катализатора крекировать н-гексан. [9]
После обработки восстановленных цеолитов кислородом при 350 С они вновь приобретают способность к поглощению значительных количеств оксида углерода. [10]
При обработке цеолита алюмогидри-дом лития определяется количество Н2, которое выделяется при взаимодействии LiALH4 c доступными для него молекулами Н2О или кислотными ОН-группами. Разность полученных величин дает число кислотных центров в больших полостях цеолита. [11]
При обработке цеолита 0 63 Nd NaY в токе воздуха и гелия при 500 С происходит миграция катионов неодима из больших полостей в содалитовые ячейки. Последующее прокаливание образца при 750 С приводит к обратной миграции катжн нов неодима из содалитовых ячеек в большие полости. Эти результаты показывают, что в условиях промышленного применения цеолитсодержащих катализаторов с редкоземельными элементами, вероятнее всего, катионы редкоземельных элементов располагаются в больших полостях структуры цеолитного компонента. [12]
При паровой обработке цеолитов с большой степенью обмена ( 40 %) образуются катализаторы, по свойствам близкие к так называемым ультрастабильным цеолитам, т.е. с увеличенным числом гидроксильных групп некислотного типа и с уменьшенным числом групп кислотного типа ( гл. Очевидно, этим и объясняется наличие максимума активности цеолитов при 30 % - ном обмене. [13]
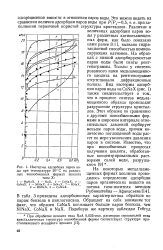 |
Изотермы адсорбции паров воды при температуре 209 С на различных ионообменных формах цеолита типа X. [14] |
При обработке цеолита типа NaA 0 025-мол. [15]
Страницы: 1 2 3 4