Образование - кристаллические зародыш
Cтраница 4
В начальный период кристаллизации NaHCO3 ( образование кристаллических зародышей) оптимальная температура поглощения СО2 находится около 50 С. При степени карбонизации / С 100 % фактором, влияющим на скорость поглощения СО2, является ее парциальное давление над карбонизуемым раствором. [46]
Поэтому в производственных условиях в зоне образования кристаллических зародышей увеличивают температуру до 60 - 65 С. [47]
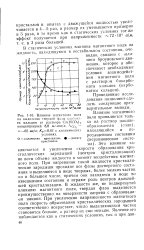 |
Влияние магнитного поля на выделение твердой фалы кар. она-та кальция ил раствора Са ( НСО3 2 концентрацией 8 0 мг-экв / л. Л со - - 62 мг / л. Яр 0 62 в динамических. [48] |
Это влияние заключается в увеличении скорости образования кристаллических зародышей ( центров кристаллизации) во всем объеме жидкости в момент воздействия магнитного поля. При нагревании такой жидкости кристаллические зародыши проходят все фазы дисперсного состояния и выделяются в виде твердых, более мелких частиц но в большем числе, причем они находятся в воде во взвешенном состоянии и играют роль центров дальнейшей кристаллизации. В жидкости же, не подвергнутой влиянию магнитного поля, твердая фаза выделяется преимущественно на поверхности нагрева с образованием накипи. При увеличении напряженности магнитного поля скорость образования кристаллических зародышей соответственно возрастает, число выделяющихся частиц становится больше, а размер их еще меньше. [49]
Поэтому в производственных условиях в зоне образования кристаллических зародышей увеличивают температуру до 60 - 65 С. [50]
Изложенные рассуждения справедливы и для случая образования кристаллических зародышей, что объясняет большую роль стенок и частичек примесей в ускорении процесса кристаллизации. Работа образования зародышей особенно снижается для частиц изоморфных примесей или кристаллических частиц, имеющих с кристаллизующимся веществом сходное строение по каким-либо граням. [51]
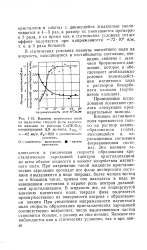 |
Влияние магнитного поля на выделение твердой фазы карбоната кальция из раствора Са ( НСО5 2 концентрацией 8 0 мг-экв / л. Дсо - - 62 мг / л. / Ср0 62 в динамических условиях. [52] |
Это влияние заключается в увеличении скорости образования кристаллических зародышей ( центров кристаллизации) во всем объеме жидкости в момент воздействия магнитного поля. При нагревании такой жидкости кристаллические зародыши проходят все фазы дисперсного состояния и выделяются в виде твердых, более мелких частиц но в большем числе, причем они находятся в воде во взвешенном состоянии и играют роль центров дальнейшей кристаллизации. В жидкости же, не подвергнутой влиянию магнитного поля, твердая фаза выделяется преимущественно на поверхности нагрева с образованием накипи. При увеличении напряженности магнитного поля скорость образования кристаллических зародышей соответственно возрастает, число выделяющихся частиц становится больше, а размер их еще меньше. [53]
В соответствии с этим уравнением скорость образования кристаллических зародышей выше определенной степени пересыщения очень быстро возрастает. Качественно экспериментальные данные согласуются с теоретическими. [54]
Последние два соотношения выполняются и при образовании кристаллических зародышей, например при осаждении свинца и серебра на платину. [55]
Процесс кристаллизации характеризуется двумя видимыми периодами: образованием мельчайших кристаллических зародышей - центров кристаллизации - и их ростом. [56]
Ад-атомы в процессе электрокристаллизации участвуют или в образовании кристаллических зародышей, или в их росте. При этом атомы должны принять ориентированное положение в кристаллической решетке. Торможение в этой стадии электродного процесса сопровождается возникновением перенапряжения. [57]
Процесс кристаллизации из растворов включает две стадии: образование кристаллических зародышей и их дальнейший рост. [58]
Можно предположить, что повышение температуры увеличивает скорость образования кристаллических зародышей не только вследствие уменьшения их критического размера [ см. уравнение ( 4) ], но также, по-видимому, и в результате уменьшения гидратации ионов [7, 57], что облегчает их объединение в зародыш. Косвенным доказательством тому служит уменьшение содержания кристаллогидратной воды в составе выделяющейся соли по мере повышения температуры кристаллизации. [59]
Страницы: 1 2 3 4