Образование - карбокатион
Cтраница 1
Образование карбокатиона может существенным образом ускориться в результате эффекта сближения групп, обладающих я-электронными ( этиленовые двойные связи и ароматические ядра) и даже re - электронными парами. Такое ускорение называется анхимерным. [1]
Образование карбокатиона может быть лимитирующей стадией. Так, при бензилировании бензола и толуола в присутствии BF3 в алканах ив избытке арена реакция имеет нулевой порядок по субстрату, первый порядок по бензилхлориду и второй порядок по катализатору. [2]
Образование карбокатионов в газовой фазе в результате ионизации RX на ионы R и Х - представляет собой эндотермический процесс, который характеризуется очень высокой положительной энтальпией. [3]
Образование карбокатионов из парафиновых, нафтеновых и олефиновых углеводородов может идти и по ассоциативному и по диссоциативному механизмам. [4]
Образование карбокатионов в газовой фазе в результате ионизации RX на ионы R и X представляет собой эндотермический процесс, который характеризуется очень высокой положительной энтальпией. [5]
Образование предпочтительно первого карбокатиона и означает присоединение по правилу Марковникова. [6]
Для образования карбокатионов обычно необходима сильнополярная ( высокое значение е), сильно сольватирующая ионы среда. Выше уже рассматривалось каталитическое действие ионов Ag ( см. разд. [7]
Факт образования карбокатионов однозначно подтвержден методами протонно-магнитного резонанса и инфракрасной спектроскопии. [8]
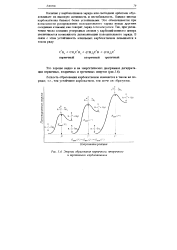 |
Энергии образования первичного, вторичного и третичного карбокатионов. [9] |
Легкость образования карбокатионов изменяется в таком же порядке, т.е., чем устойчивее карбокатион, тем легче он образуется. [10]
При образовании карбокатиона резонанс невозможен, а приобретенный заряд ничем не компенсируется. Так, длина связи С - С1 в винильных и ариль-ных системах равна 1 73 А, что можно сравнить со значением 1 78 А для связи С - С1 в насыщенных системах. При прочих равных условиях более короткая связь является более прочной. [11]
Энергия активации образования карбокатиона будет тем меньше, чем более стабилизирован этот катион электроно-донорными группами. Таким образом, в ряду Кперв RBTop - трет склонность к реакциям SN1 будет возрастать. Особенно заметное стабилизирующее действие на положительно заряженный углеродный атом оказывает соседняя ненасыщенная группировка. [12]
Энергия активации образования карбокатиона будет тем меньше, чем более стабилизирован этот катион электроно-донорными группами. Таким образом, в ряду Нперв RBTOP Ripei склонность к реакциям SN1 будет возрастать. Особенно заметное стабилизирующее действие на положительно заряженный углеродный атом оказывает соседняя ненасыщенная группировка. [13]
Реакция начинается с образования карбокатиона а нормального строения, который превращается в карбокатион б изостроения в результате изомеризации углеродной цепи, заключающейся в перемещении метильной группы. Это перемещение происходит через переходную стадию циклического карбокатиона в, в котором перекрывание гибридной атомной орбитали метильной группы с атомными ор биталями двух других атомов углерода приводит к образованию молекулярной орбитали, общей для трех атомов углерода. [14]
Согласно [218], образование карбокатионов имеет две стадии. Первая стадия быстрая ( она завершается за время действия импульса длительностью 40 - 80 не); вторая - более медленная, причем она подчиняется закону псевдопервого порядка для всех использованных концентраций ароматических соединений. [15]
Страницы: 1 2 3 4